题目内容
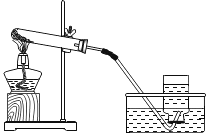
【题目】如下图表示电解水的简易装置。请回答下列问题:
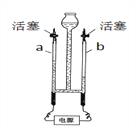
(1)水中共含有______ 种元素;
(2)与a试管中的电极相连的是电池______(填“正”或“负”)极;
(3)a试管和b试管中的气体的体积之比约等于_______;
(4)电解水反应的化学式表达式为_____________________,属于基本反应类型的__________。
(5)计算水中氧元素的质量分数是________(写出计算过程,保留一位小数)。
【答案】2 正 1:2 H2O ![]() H2+O2 分解 1×2+16×1=18 ,
H2+O2 分解 1×2+16×1=18 , ![]() =88.9%
=88.9%
【解析】
本题考查了水的电解实验及水中氧元素的质量分数。
(1)水中共含有2种元素;
(2)图示的电解水实验中可看到:b试管内气体约为a管内气体体积的2倍,则a管内为氧气,与a管相连的试管为电源的正极;
(3)图示中b管内氢气的体积约为a管内氧气体积的2倍,a试管和b试管中的气体的体积之比约等于1:2;
(4)水在通电条件下可分解为氢气和氧气,反应的化学式表达式为:H2O ![]() H2+O2
H2+O2
,该反应为一种物质生成两种物质的分解反应;
(5)水的相对分子质量=1×2+16×1=18;水中氧元素的质量分数=![]() ×100%=88.9%
×100%=88.9%

【题目】日常生活中,我们常饮用桶装水网上盛传“千沸水”(指反复多次烧开的水)中含有大量亚硝酸盐,摄入一定量可导致中毒此外,亚硝酸盐在人体内还能形成强致癌性物质一亚硝胺,饮用会致癌。这是真的吗?
问题:加热次数对亚硝酸盐含量是否有影响?
查阅资料:我国在《GB19298-2003瓶(桶)装饮用水卫生标准》中对亚硝酸盐(以NO2计)的含量规定为小于5μg/L。
进行实验:(1)取新鲜的桶装水放置在饮水机上,测定36h内反复加热(共计181次)的水样,亚硝酸盐含量(以NO2计)检测结果如下表:
加热时间/h | 0 | 1 | 3 | 6 | 12 | 24 | 36 |
含量/g/L | 0.67 | 0.73 | 1.12 | 1.23 | 1.81 | 2.44 | 3.53 |
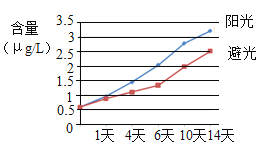
(2)取检验合格的14桶桶装水分两组(每组7份)静态放置,进行存放环境检测,亚硝酸盐含量(以NO22.5计)检测结果如图。
已知人在日常生活中主要摄取亚硝酸盐的途径是蔬菜,通过人体唾液的转化,间接进入人体的亚硝酸盐含量最高在300mg/kg,人并没有因为食用蔬菜而导致亚硝天酸盐中毒,由此可知“千沸水”中的亚硝酸盐不足以使人中毒。没有明确证据证明亚硝酸盐能致癌,在正确使用饮水机的前提下,“千沸水”不会致癌。反复煮沸的水,只是活性降低了,不易被人体细胞吸收。
请依据以上文章内容,回答下列问题:
(1)依据表中数据,煮沸的水中亚硝酸盐含量的变化规律是____________________。
(2)依据图可知,存放桶装水时,为降减低亚硝酸盐的产生需采取的措施是________。
(3)你认为“千沸水”可以饮用吗?说明理由__________________________________。
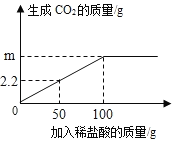
【题目】化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用20g石灰石样品,把80g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如右表:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入20g | 15g |
第二次加入20g | 10g |
第三次加入20g | 5g |
第四次加入20g | 3g |
(1)石灰石样品中碳酸钙的质量分数为_________;
(2)第一次实验参加反应的碳酸钙的质量为__________g;
(3)计算第一次加入20g稀盐酸充分反应后生成二氧化碳的质量为_________。(写出计算过程)