题目内容
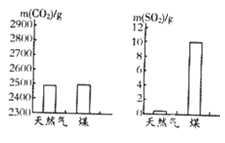
【题目】一定条件下,5.6gC2H4与17.6gO2恰好完全反应,生成7.2gH2O、13.2gCO2和物质X.则X的质量为________,该反应中C2H4与X的化学计量数之比为________ .
【答案】2.8g 2:1
【解析】
根据质量守恒定律,反应前后质量总和不变,X的质量=(5.6g+17.6g)-(7.2g+13.2g)=2.8g;
5.6gC2H4中含有碳元素质量=![]() ,含有氢元素质量=5.6g-4.8g=0.8g,
,含有氢元素质量=5.6g-4.8g=0.8g,
水中含有氢元素质量=![]() ,含有氧元素质量=7.2-0.8g=6.4g;
,含有氧元素质量=7.2-0.8g=6.4g;
二氧化碳中含有碳元素质量=![]() ,含有氧元素质量=13.2g-3.6g=9.6g;
,含有氧元素质量=13.2g-3.6g=9.6g;
所以X中含有的碳元素质量=4.8-3.6g=1.2g,含有的氧元素质量=17.6-9.6g-6.4g=1.6g,
所以原子个数比=![]() ,所以X是CO;
,所以X是CO;
C2H4、氧气、二氧化碳、水、一氧化碳的分子个数比为:![]() ;将C2H4燃烧的方程式配平得:
;将C2H4燃烧的方程式配平得:
4C2H4+11O2![]() 6CO2+8H2O+2CO,该反应方程式中C2H4与X化学计量数之比=2:1。
6CO2+8H2O+2CO,该反应方程式中C2H4与X化学计量数之比=2:1。

【题目】M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动。
(提出问题)M、铜、铝的金属活动性顺序是怎样的?
(猜想与假设)小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是_____.
(设计与实验一)小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸);
实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu;_____ |
几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | _____ |
(交流与表达)同学们对同一实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中无气泡产生的原因,该原因_____.
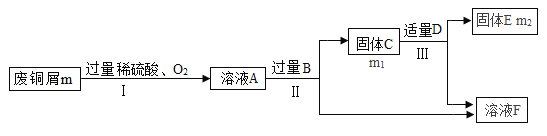
(设计与实验二)为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
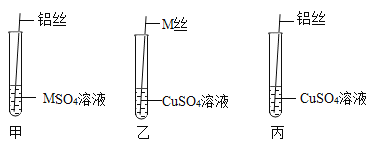
(1)试管乙中观察到的现象是_____.
(2)试管丙中发生反应的化学反应方程式_____
(交流与表达)同学们经讨论后认为该实验可以优化,去掉试管_____ (填试管编号)中的实验,也可以得出正确的结论。