题目内容
【题目】回收利用废旧金属是保护金属资源的有效途径之一。利用废旧铜屑(假设只含Cu、Zn)制取金属铜,并得到硫酸锌溶液,主要流程如图所示(反应条件已略去)
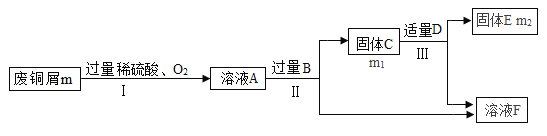
已知:2Cu+2H2SO4+O2![]() 2CuSO4+2H2O,假定制取过程中金属无损失。则
2CuSO4+2H2O,假定制取过程中金属无损失。则
(1)溶液A含有的溶质有_______种。
(2)固体C的成分为_______。
(3)过程Ⅰ,Ⅲ中有发生同一个反应发生,该反应的化学方程式为 _______ .
(4)废铜屑中锌的质量分数是______(用m、m1、m2表示)。
【答案】3 Cu和Zn Zn+ H2SO4 == ZnSO4 + H2↑ ![]()
【解析】
(1)氧化铜和硫酸反应生成硫酸铜和水,锌和硫酸反应生成硫酸锌和氢气,以及加入的硫酸是过量的,所以溶液A中含有的溶质有3种;故填:3.
(2)溶液A中的硫酸铜和过量的B(锌)反应,生成铜和硫酸锌,固体C的成分是Cu和Zn;故填:Cu和Zn。
(3)过程Ⅰ和过程Ⅲ都发生锌和硫酸反应生成硫酸锌和氢气,反应的方程式为Zn+ H2SO4 == ZnSO4 + H2↑,故填:Zn+ H2SO4 == ZnSO4 + H2↑。
(4)由题意可知m2是铜的质量,则废铜屑中锌的质量为m-m2,废铜屑中锌的质量分数是![]() ;故填:
;故填:![]() 。
。

【题目】一定条件下,5.6gC2H4与17.6gO2恰好完全反应,生成7.2gH2O、13.2gCO2和物质X.则X的质量为________,该反应中C2H4与X的化学计量数之比为________ .
【题目】铜、铁是人类使用最早、应用广泛的金属.
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
(1)上述制品不涉及到的材料是______(选填序号).
A、金属材料 B、无机非金属材料 C、复合材料
(2)如图1为出土文物古代青铜铸件“马踏飞燕”.该文物能保存至今的原因可能是_____(选填序号).
A、铜的活泼性弱 B、铜不会生锈 C、深埋于地下,隔绝空气
(二)铁、铜的冶炼
①我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式:_________,2CuO+C![]() 2Cu+CO2↑.
2Cu+CO2↑.
②铁、铜矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等.CuFeS2为二硫化亚铁铜,其中S元素的化合价为______.
(1)工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为______________.
炼铁不采用黄铁矿、黄铜矿,可能的原因是:
①黄铁矿、黄铜矿含铁量相对低;②________________________________.
(2)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4![]() 4CuSO4+2Fe2(SO4)3+2H2O.
4CuSO4+2Fe2(SO4)3+2H2O.
向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
①发生主要反应的化学方程式:Fe+Fe2(SO4)3=3FeSO4,________________________.
②FeSO4溶液经蒸发浓缩、___________、过滤等操作得到FeSO47H2O晶体.
(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe2O3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO4、Fe2(SO4)3溶液.向溶液中加入过量NaOH溶液得到Cu(OH)2、Fe(OH)3固体.
(1)证明NaOH溶液过量的方法:静置,向上层清液中滴加________溶液,无现象.
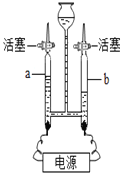
(2)用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH)2分解为CuO;在500℃时,Fe(OH)3分解为Fe2O3.
②在1400℃时,CuO分解为Cu2O和O2,Fe2O3分解为复杂的铁的氧化物和O2.
(1)装配好实验装置后,先要________________.
(2)停止加热后仍需继续通N2,可防止倒吸和______________________________.
(3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
温度/℃ | 室温 | 100 | 550 | 1400 |
B装置/g | 200.00 | 201.80 | 205.04 | 205.04 |
C中铜网/g | 100.00 | 100.00 | 100.00 | 101.28 |
①此黄铜矿中铜、铁元素的质量分数:ω(Cu)%=________;ω(Fe)%=__________.
②复杂的铁的氧化物化学式为__________.