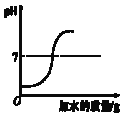题目内容
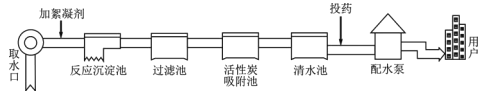
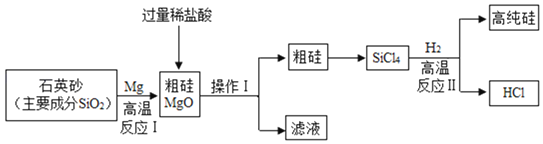
【题目】如图是一种制备高纯硅的工艺流程图:
(查阅资料)常温下,氯化镁溶液呈中性。
![]() 反应I的化学方程式:
反应I的化学方程式:![]() ,该反应属于______
,该反应属于______![]() 填基本反应类型
填基本反应类型![]() 。反应II要在无氧气环境中进行,原因是______
。反应II要在无氧气环境中进行,原因是______![]() 答出一种即可
答出一种即可![]() 。
。
![]() 操作I的名称是______,滤液中的溶质为______
操作I的名称是______,滤液中的溶质为______![]() 填化学式
填化学式![]() 。
。
![]() 上述生产流程中,可以循环利用的物质是______
上述生产流程中,可以循环利用的物质是______![]() 填化学式
填化学式![]() 。
。
【答案】置换反应 防止氢气和氧气混合而爆炸 过滤 HCl和![]() HCl
HCl
【解析】
![]() 反应I的化学方程式:
反应I的化学方程式:![]() ,由一种单质和一种化合物反应生成新的单质和新的化合物的反应是置换反应,符合置换反应的特征,属于置换反应。反应II要在无氧气环境中进行,原因是防止氢气和氧气混合而发生爆炸。
,由一种单质和一种化合物反应生成新的单质和新的化合物的反应是置换反应,符合置换反应的特征,属于置换反应。反应II要在无氧气环境中进行,原因是防止氢气和氧气混合而发生爆炸。
![]() 操作I实现了固体和液体的分离,为过滤。由于加入的盐酸过量,且盐酸和氧化镁反应生成氯化镁,所以滤液中的溶质为剩余的HCl和生成的
操作I实现了固体和液体的分离,为过滤。由于加入的盐酸过量,且盐酸和氧化镁反应生成氯化镁,所以滤液中的溶质为剩余的HCl和生成的![]() 。
。
![]() 由工艺流程图可知,上述生产流程中,HCl既是反应物又是生成物,所以可以循环利用的物质是 HCl。
由工艺流程图可知,上述生产流程中,HCl既是反应物又是生成物,所以可以循环利用的物质是 HCl。
故答案为:
![]() 置换反应;防止氢气和氧气混合而爆炸。
置换反应;防止氢气和氧气混合而爆炸。
![]() 过滤;HCl和
过滤;HCl和![]() 。
。
![]() 。
。

【题目】小维与家人聚餐时,对火锅燃料“固体酒精”产生了好奇,于是他与同学对其成分进行如下探究。
(查阅资料)(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的。
(2)氯化钙、氯化钡溶液均呈中性。
(提出问题)(1)酒精中是否含有碳元素? (2)固体酒精中氢氧化钠是否变质?
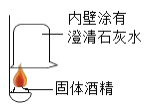
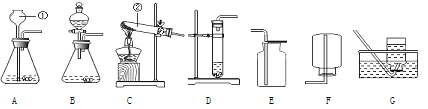
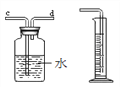
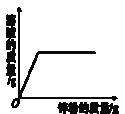
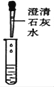
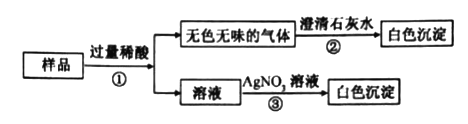
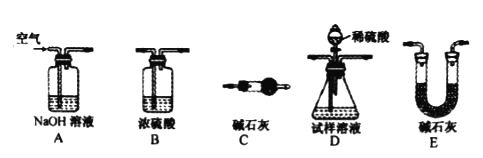
(实验探究)(1)如图所示进行实验,发现澄清石灰水_____,可得出酒精中含有碳元素的结论。
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,请用化学方程式表示该沉淀是如何形成的:_____,由此说明氢氧化钠已变质。
(实验结论)(1)酒精中含有碳元素。 (2)固体酒精中氢氧化钠己经变质。
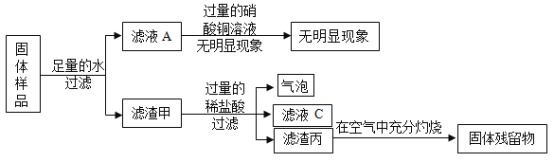
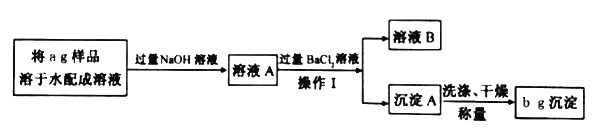
(拓展延伸)为进一步确定氢氧化钠的变质程度,分组进行探究。甲组同学取烧杯上层清液于两支试管中,按如图所示进行实验。
实验方案 |
|
|
实验现象 | 溶液_____ | 产生白色沉淀 |
实验结论 | 清液中有氢氧化钠 | 清液中有____ |
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是_____。他们另取烧杯中的上层清液,加足量氯化钡溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红,证明清液中一定有氢氧化钠。
(反思交流)乙组实验中加足量氯化钡溶液的目的是_____。
(实验结论)小组同学经过讨论,一致认为该固体酒精中的氢氧化钠部分变质。