题目内容
【题目】氯化铁(FeCl3)溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响。写出本实验发生反应的文字表达式______________。
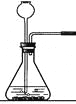
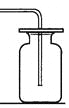
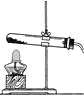
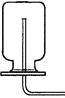
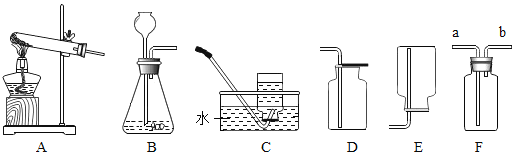
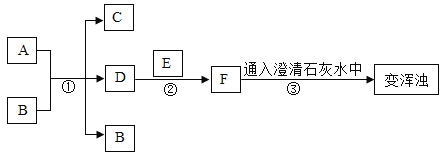
(1)分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,如图观察到________________,就可以粗略判断,得出实验结果。为进一步判断上述实验结论的准确性,运用如图,小刚同学进行了如下实验方案设计。
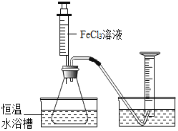
(2)[方案一]在不同过氧化氢浓度下,测定收集相同体积的气体所需时间;
[方案二]在不同过氧化氢浓度下,测定____________;
物理量 实验序号 | 30%H2O2溶液的体积(mL) | 2%FeCl3溶液的体积(mL) | 加入H2O的体积(mL) | 反应的时间(min) | 生成O2的体积(mL) |
1 | 5 | x | 20 | 5 | V1 |
2 | 10 | 3 | 15 | y | V2 |
方案二的实验测量结果:
①表中x=____,y=____.
②实验结论:通过测量,若V1___V2(填“>”“=”或“<”),说明___________.
(3)除了过氧化氢浓度之外,还有哪些因素能影响它分解生成氧气的速率?请任意选择一种并写出实验方案_____________。
【答案】过氧化氢![]() 水+氧气 气泡生成的速度 相同时间收集的气体的体积 3 5 < 相同条件下,过氧化氢溶液浓度越大分解越快 催化剂的质量;常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入不同质量的MnO2,然后将锥形瓶分别放于相同温度的水中,测量各生成一瓶(相同体积)O2 所需的时间(答案合理即可)
水+氧气 气泡生成的速度 相同时间收集的气体的体积 3 5 < 相同条件下,过氧化氢溶液浓度越大分解越快 催化剂的质量;常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入不同质量的MnO2,然后将锥形瓶分别放于相同温度的水中,测量各生成一瓶(相同体积)O2 所需的时间(答案合理即可)
【解析】
解:过氧化氢在氯化铁溶液的催化下生成水和氧气,对应的文字表达式:过氧化氢![]() 水+氧气;
水+氧气;
(1)可以通过气泡生成的速度,就可以粗略判断,得出实验结果;
(2)[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间;
[方案二]在不同过氧化氢浓度下,测定相同时间收集的气体的体积;
①方案二的实验测量结果(这个数据要看的懂才能很好理解,选用的是同一种质量分数的过氧化氢溶液,不同的体积,但是采取加入水而最后溶液的体积还是相等的,也就是表格中第二列和第四列之和相等,此时溶液体积相等,但是溶质的质量分数不同,由于是不同浓度下的过氧化氢,所以加入的氯化铁溶液体积也应该相同,相同时间产生的氧气的体积多少,所以反应时间也相同)所以表中x=3,y=5
②实验结论:通过测量,若V1<V2(填“>”“=”或“<”),说明 反应物的浓度越高,反应速度越快;
(3)催化剂的质量可能影响它分解生成氧气的速率;方案:常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入不同质量的MnO2,然后将锥形瓶分别放于相同温度的水中,测量各生成一瓶(相同体积)O2 所需的时间。

【题目】化学实验是学习化学和进行科学研究的重要方法和途径。学会气体物质的制备方法是研究气体、利用气体的基础。请根据下图回答有关问题:
|
|
|
|
|
|
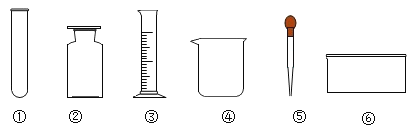
① | ② | ③ | ④ | ⑤ | ⑥ |
(1)在常温下实验室欲制取氧气所选用的装置是 (填序号),为了便于调控反应的进行,可以对发生装置进行改进,请简要说明你的改进措施 。
(2)从上述仪器中选择一种你比较熟悉的仪器,写出它的名称 ,简要写出它的用途 。
(3)同学们以“化学反应中,反应物与生成物的质量关系”为课题进行探究。经讨论分析、查阅资料后设计了A、B两套实验装置,并在实验过程中做到操作规范、准确称量和细致观察。实验完毕后,使用A装置进行实验得到的结果是:反应前后反应物的总质量与生成物的总质量相等;而使用B装置进行实验得到的结果是:反应前后反应物的总质量与生成物的总质量不相等。请你分析导致出现两种不同结果的原因是
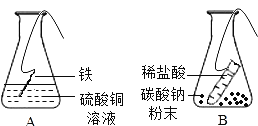
写出B装置中发生反应的化学方程式 -。