题目内容
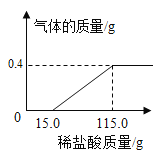
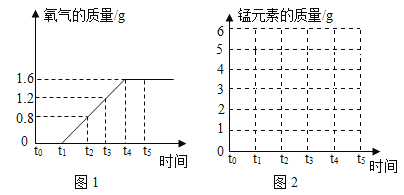
【题目】实验室制取氧气(2KMnO4![]() K2MnO4+MnO2+O2↑)时,某同学取质量为x的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图1所示,请回答下列问题。
K2MnO4+MnO2+O2↑)时,某同学取质量为x的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图1所示,请回答下列问题。
(1)计算高锰酸钾(KMnO4)的相对分子质量=_____。
(2)t0~t1质量都不变的原因是_____。
(3)t4~t5质量都不变的原因是_____。
(4)请根据图1中数据计算高锰酸钾的质量x为多少_____?(写出计算过程)
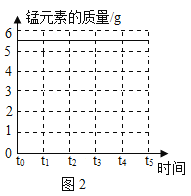
(5)请在图2坐标中,画出固体中锰元素质量在t0~t5时段的变化示意图_____。
【答案】158 高锰酸钾分解需要达到一定的温度 高锰酸钾已经完全反应 15.8g 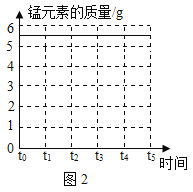
【解析】
根据生成的氧气的质量和对应的化学方程式求算高锰酸钾的质量。
(1)高锰酸钾(KMnO4)的相对分子质量=39+55+16×4=158。
(2)由于需要达到一定温度才能分解,所以t0~t1质量都不变。
(3)t4~t5质量都不变的原因是 高锰酸钾已经完全反应。
(4)高锰酸钾的质量为x,设锰元素的质量为y
根据2KMnO4![]() K2MnO4+MnO2+O2↑可得关系式为
K2MnO4+MnO2+O2↑可得关系式为
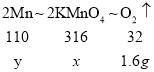
![]()
x=15.8g
y=5.5g
(5)由于过程中锰元素质量不变,且在固体中,固体中锰元素质量在t0~t5时段的变化示意图。

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
相关题目