题目内容
【题目】学习氢氧化钠的化学性质后,小明做了如下实验,请你补充完整:(提示:氯化镁溶液为无色,不能使酚酞溶液变红)
实验 | 实验操作 | 实验现象 | 结论或解释 |
(1) |
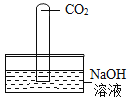
| 现象为________ | 二氧化碳与氢氧化钠发生化学反应 |
(2) |
| 溶液由无色变为红色 | 结论为________ |
(3) |
| 加人稀盐酸后,未观察到明显现象;滴人酚酞后,溶液变红色 | 盐酸与氢氧化钠未发生化学反应 |
(4) |
| 有白色沉淀生成 | 生成沉淀的原因(用化学方程式解释)_______ |
(5)小军认为小明实验(1)操作设计不足以说明二氧化碳与氢氧化钠发生化学反应,应做的改进是________;小军还认为小明实验(3)的结论不正确。
(6)将(2)(3)(4)实验后试管中的物质倒人一个洁净的烧杯中,烧杯中有白色沉淀,静置,上层清液无色,据此可知上层清液中溶质的成分一定有(除指示剂外)________,为了检验可能存在的溶质,你的实验方案是________。
【答案】试管内液面上升 氢氧化钠溶液呈碱性,能使酚酞溶液变红 ![]() 另取一套相同的装置 ,将氢氧化钠溶液改为等体积的水,做对比实验 NaCl 取少量上层清液于试管中,滴入氢氧化钠溶液,观察是否产生白色沉淀(合理即可)
另取一套相同的装置 ,将氢氧化钠溶液改为等体积的水,做对比实验 NaCl 取少量上层清液于试管中,滴入氢氧化钠溶液,观察是否产生白色沉淀(合理即可)
【解析】
(1)二氧化碳与氢氧化钠反应,试管内气压减小,试管内液面上升;
(2)由于溶液由无色变为红色,可知氢氧化钠溶液呈碱性,能使酚酞溶液变红;
(4)氢氧化钠与氯化镁反应生成氢氧化镁白色沉淀和氯化钠;
故填:试管内液面上升;氢氧化钠溶液呈碱性,能使酚酞溶液变红;2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
(5)由于二氧化碳能溶于水,故不足以说明二氧化碳与氢氧化钠发生化学反应,可换用等体积的水做对比实验的方法;故填:另取一套相同的装置 ,将氢氧化钠溶液改为等体积的水,做对比实验;
(6)实验结束后,将(2)(3)(4)三支试管中的物质倒入一只洁净的烧杯中,烧杯中出现白色沉淀,静置,上层清液无色;溶质可能两种:①NaCl、②NaCl和MgCl2,即一定含有氯化钠,可能含有氯化镁;取少量上层清液于试管中,滴加氢氧化钠溶液,出现白色沉淀,证明含有氯化镁。
故填:NaCl;取少量上层清液于试管中,滴入氢氧化钠溶液,观察是否产生白色沉淀(合理即可)。

 阅读快车系列答案
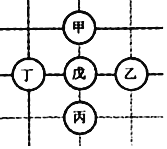
阅读快车系列答案【题目】如图所示,围棋棋盘上有五枚棋子,代表铁、稀盐酸、氢氧化钡、碳酸钙、硝酸银五种物质,相邻棋子间的连线表示物质间可以反应。已知与戊的反应中:甲﹣戊的反应类型不同于其它几个反应;丙﹣戊反应能产生一种气体,且该气体还能与丁反应生成沉淀。则下列对应关系正确的是( )
甲 | 乙 | 丙 | 丁 | 戊 | |
A | 铁 | 硝酸银 | 碳酸钙 | 氢氧化钡 | 稀盐酸 |
B | 硝酸银 | 铁 | 稀盐酸 | 氢氧化钡 | 碳酸钙 |
C | 硝酸银 | 铁 | 碳酸钙 | 氢氧化钡 | 稀盐酸 |
D | 铁 | 氢氧化钡 | 碳酸钙 | 硝酸银 | 稀盐酸 |
A. A B. B C. C D. D
【题目】氯化钠的部分溶解度如下:
温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
溶解度/g | 35.8 | 36.0 | 36.1 | 36.4 | 37.1 | 38.0 | 39.21 |
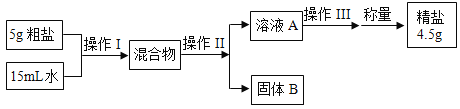
(1)20℃时,15g水中溶解_____g氯化钠刚好形成饱和溶液。
(2)粗盐(含有泥沙的氯化钠)提纯的实验过程如图所示,溶液A是_____(填“饱和”或“不饱和”)溶液,操作Ⅱ是_____。