题目内容
某校研究性学习小组在学习了双氧水分解制氧气的实验后,知道催化剂(Mn02,)能改变化学反应速率。到底Mn02是不是该反应的催化剂以及还有哪些因素与化学反应速率有关呢?
【小组讨论】:小明同学观点:化学反应速率与反应物的质量分数有关;
小红同学观点:化学反应速率与反应温度有关;
小峰同学观点:化学反应速率与 有关。
【设计实验】:为了验证他们的观点,设计并进行了以下实验:
(1)请你写出实验中所发生的化学反应方程式 ;
(2)____实验证明小明的观点是正确的,_______实验证明小红的观点是正确的。
| A.①和② | B.②和③ | C.③和④ | D.①和④E.②和⑤ |
(4)加入Mn02后,H202分解的速率大大提高,为了证明Mn02是该反应的催化剂,必须检验其质量没有改变,可通过 (填操作名称)将其分离出来称量,同时还应检验其 没有改变。
催化剂的质量;2H2O2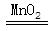 2H2O+O2↑;BD;越快,过滤,化学性质
2H2O+O2↑;BD;越快,过滤,化学性质
解析试题分析:由他们设计的实验可知催化剂的质量分布取用了0.1g和0.2g,即小峰的观点是化学反应速率与催化剂的质量有关;过氧化氢分解生成的水和氧气,反应的化学方程式为:2H2O2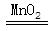 2H2O+O2↑;小明同学观点是化学反应速率与反应物的质量分数有关,那采取控制变量法应选择不同浓度的过氧化氢溶液,其他条件均相同的实验组,及②和③ ;小红同学观点是化学反应速率与反应温度有关,那就选择温度不同,但其他条件相同的实验组,即①和④ ;对比②和③、①和④可知:反应温度越高或反应物的质量分数越大,则反应速率快;过滤可将液体和固体分离;判断一种物质是否是某反应的催化剂,要看它是否具备催化剂的特征,即“一变二不变”: 能否改变反应的速率;反应前后本身的质量,是否改变;本身的化学性质是否改变。
2H2O+O2↑;小明同学观点是化学反应速率与反应物的质量分数有关,那采取控制变量法应选择不同浓度的过氧化氢溶液,其他条件均相同的实验组,及②和③ ;小红同学观点是化学反应速率与反应温度有关,那就选择温度不同,但其他条件相同的实验组,即①和④ ;对比②和③、①和④可知:反应温度越高或反应物的质量分数越大,则反应速率快;过滤可将液体和固体分离;判断一种物质是否是某反应的催化剂,要看它是否具备催化剂的特征,即“一变二不变”: 能否改变反应的速率;反应前后本身的质量,是否改变;本身的化学性质是否改变。
考点:影响化学反应速率的因素及催化剂的性质

老师请化学兴趣小组的同学帮助他将失去标签的碳酸钠、稀盐酸、氯化钠、氢氧化钠和氯化钙溶液鉴别出来.重新贴好标签.为了区分这五种溶液,将试剂瓶编号为A,B,C,D,E,该小组同学进行了如下探究:
| | 实验步骤 | 实验现象 | 实验结论 |
| 步骤一 |  | B,C溶液呈现红色 A,D,E溶液颜色无明显变化 | B,C溶液显 性 |
| 步骤二 | 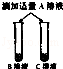 | B,C溶液红色均消失, 且C溶液中产生大量气泡 | 可确定B为 溶液;A与C的反应通常 不用作实验室制取气体的 原因是 |
| 步骤三 |  | E中无明显现象, D中的现象为 | 确定E为氯化钠溶液, 则D溶液与所加试剂发生反应的化学方程式为 |
以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
(1)通过实验①和②对比可知,化学反应快慢与 有关;
(2)通过对比实验 和 可知,化学反应快慢与温度的关系是 。
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是 。
在学习过程中,可以判断反应发生的方法有多种。
(1)向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应。
(2)在图的实验中,当观察到的现象是 就可证明NaOH与HCl发生了反应。

(3)不使用指示剂或pH试纸等方法,也可证明反应发生。向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该合理的物质是 。