题目内容
【题目】某校化学兴趣小组就空气中氧气的含量进行了如下实验探究:
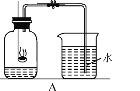
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体。他们应该选择________ (填序号),为了充分消耗容器中的氧气,药品的用量应保证足量 。
A.蜡烛 B.红磷 C.硫 D.木炭
(2)小组同学共同设计如图所示的装置,为了确保实验的成功,在装药品之前应该____,写出集气瓶内反应的文字表达式:____
(分组实验)在讨论的基础上,他们分组进行了实验。
(数据分析)实验结束后,整理数据如下表:(注:集气瓶容积为 100 mL)
组别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积/mL | 20 | 21 | 19 | 20 | 22 | 18 |
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的____。通过实
验还可以推断出集气瓶中剩余气体的性质是____、____(写出两点)。
(4)实验测量值比真实值小的原因可能是:①____量不足;②装置气密性____;③未冷却至____就打开止水夹。
【答案】B检查装置的气密性红磷+氧气![]() 五氧化二磷1/5不溶于水 不支持燃烧红磷差室温
五氧化二磷1/5不溶于水 不支持燃烧红磷差室温
【解析】
(1)A.蜡烛与氧气反应能生成二氧化碳气体,与要求不符,选项错误;B.红磷与氧气反应生成五氧化二磷固体,符合题目要求,选项正确;C.硫与氧气反应生成二氧化硫气体,与题目要求不符,选项错误;D.木炭与氧气反应生成二氧化碳气体,不符合题目要求,选项错误,故选B。(2)如果装置气密性较差,瓶外的气体会进入瓶内,会造成实验结果出现错误,故要检查装置的气密性;瓶内的反应是红磷与氧气反应生成五氧化二磷,所以文字表达式写为红磷+氧气 ![]() 五氧化二磷。(3)通过表中数据分析,各小组的平均数值为20mL,即氧气的体积为20mL,所以氧气约占空气体积的1/5;反应后剩余气体的量不变,证明剩余气体即不溶于水,也不能燃烧,还不能与红磷反应,故填不溶于水,不支持燃烧。(4)如果红磷的量不足,反应后会剩余氧气,造成计算结果偏小;如果装置气密性差,瓶外的气体就会进入瓶内,测得氧气的体积会偏小,造成实验结果偏小;因为反应放热,剩余气体体积膨胀,如果不冷却就打开止水夹,求得的氧气体积就会偏小,从而造成实验结果偏小,故应冷却至室温再打开止水夹。
五氧化二磷。(3)通过表中数据分析,各小组的平均数值为20mL,即氧气的体积为20mL,所以氧气约占空气体积的1/5;反应后剩余气体的量不变,证明剩余气体即不溶于水,也不能燃烧,还不能与红磷反应,故填不溶于水,不支持燃烧。(4)如果红磷的量不足,反应后会剩余氧气,造成计算结果偏小;如果装置气密性差,瓶外的气体就会进入瓶内,测得氧气的体积会偏小,造成实验结果偏小;因为反应放热,剩余气体体积膨胀,如果不冷却就打开止水夹,求得的氧气体积就会偏小,从而造成实验结果偏小,故应冷却至室温再打开止水夹。

 全优点练单元计划系列答案
全优点练单元计划系列答案