题目内容
【题目】空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。下图是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题

(1)空气中氮气的体积分数是__________。
(2)步骤①中发生的是_________(选填“物理”或“化学”)变化。
(3)写出步骤③中发生反应的符号表达式______________________________。催化剂在反应前后,可__________反应速率,本身的质量和____________________不变。
(4)上述化学反应中属于化合反应的有________个。
(5)右图是化肥硝酸铵包装袋上的部分说明,硝酸铵应具有的性质是______(填序号)
①易溶于水 ②熔点高 ③受热易分解
【答案】78%物理![]() 改变,化学性质3①③
改变,化学性质3①③
【解析】
(1)空气中氮气的体积分数是78%,氧气的体积分数是21%;
(2)步骤①中没有产生新物质,所以是物理变化;
(3)步骤③中,氨气和氧气通过催化剂、加热的条件生成了一氧化碳和水,表达式是![]() ,催化剂的特征是反应前后质量和化学性质不变,但可以改变反应速率,速率可能加快,也可能减慢;
,催化剂的特征是反应前后质量和化学性质不变,但可以改变反应速率,速率可能加快,也可能减慢;
(4)反应②、④和⑤是化合反应,由两种或两种以上的物质反应生成一种新物质的反应;
(5)硝酸铵需要密封保存,且需要防潮,说明硝酸铵易溶于水,需要隔绝热源说明硝酸铵受热易分解。

 心算口算巧算一课一练系列答案
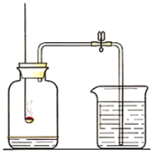
心算口算巧算一课一练系列答案【题目】(1)小明为验证质量守恒定律,做了镁粉在空气燃烧的实验(如图1),该反应的化学方程式是________。实验结束,他发现镁粉在空气中充分燃烧后,产物中还有少量黄色固体。为了弄清黄色固体的成分,小明进行了如下实验探究:
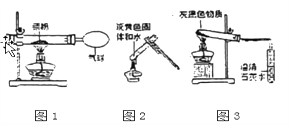
(2)(查资料1)
镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体。
氮化镁可与水剧烈反应产生氨气,该气体能是湿润的红色石蕊试纸变蓝。
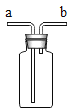
(设计实验)小明用图2所示的实验(部分操作没有画出),验证黄色固体为Mg3N2, 请完成下列实验报告。
(交流与思考)小明发现久置的镁条上有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物种呢?他叫来了小亮、小红一起进行了实验探究:
操作步骤 | 实验现象 | 实验结论 |
取少量黄色固体于试管中,加入适量水,加热,并将湿润的红色石蕊试纸放在试管口 | ___________ | 黄色固体为Mg3N2 |
(3)(猜想)小明认为可能是MgO;小亮认为可能是Mg2(OH)2CO3;小红认为可能是 Mg(OH)2。
小红认为小明的猜想是错误的,其理由是________。
(4)(查阅资料2)
Mg(OH)2受热分解产生两种氧化物。
② Mg2(OH)2CO3受热分解产生三种氧化物。
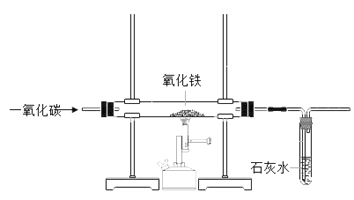
(实验探究)小亮进行实验(见图3),发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体。
(实验分析)实验后,小亮认为小红的猜想也是错误的,其理由是________。
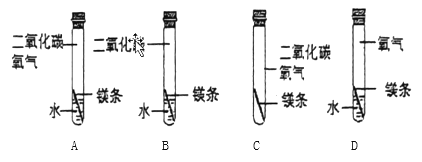
(5)(实验反思)要验证小亮的猜想,实际上只需证明黑色“外衣”想形成是否需要二氧化碳即可。为了证明这一猜想,需要进行如下图所示实验中的________(填序号,下同)和________。