题目内容
【题目】已知某白色固体混合物A中可能含有MgCl2、BaCl2、Na2SO4、NaOH、CaCO3五种物质中的两种或多种。小路同学想分析其成分,她进行了实验探究,实验过程及出现的现象如下图所示:(设实验过程中所有可能发生的反应均恰好完全反应)
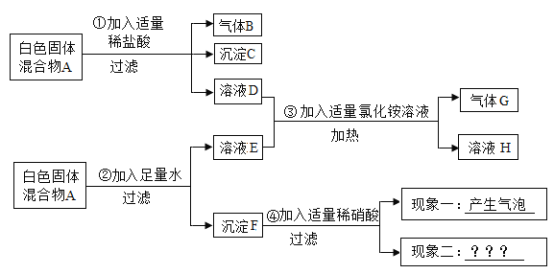
根据上述实验信息和分析推理,试回答下列问题:
(1)沉淀C的化学式为______,气体G的化学式为_______。
(2)上图中现象二为(至少答一条)____________。
(3)溶液D中肯定大量存在的阴离子是(写离子符号)_________。
(4)步骤②中发生反应的化学方程式为_______。
(5)步骤③中可能发生反应的一个化学方程式为____。
(6)由上述信息可推知,固体混合物A中一定不存在的物质是(写化学式)___你的理由是____。
【答案】BaSO4 NH3 固体部分溶解(或有未溶解的固体,或上清液呈无色,其他合理答案酌情给分) Cl- ![]()
![]() (或
(或![]() ) MgCl2 由图可知,步骤③中产生了NH3↑,说明溶液E和固体A中都存在NaOH,若固体A中含有MgCl2,它们会在步骤②中反应生成Mg(OH)2↓,则溶液E中将无OH-,导致步骤③中不会产生NH3↑,这与图中信息不符所以固体A中一定没有MgCl2(其他合理答案酌情给分)
) MgCl2 由图可知,步骤③中产生了NH3↑,说明溶液E和固体A中都存在NaOH,若固体A中含有MgCl2,它们会在步骤②中反应生成Mg(OH)2↓,则溶液E中将无OH-,导致步骤③中不会产生NH3↑,这与图中信息不符所以固体A中一定没有MgCl2(其他合理答案酌情给分)
【解析】
实验过程中所有可能发生的反应均恰好完全反应,白色固体混合物A中加入适量稀盐酸,可得到气体B、沉淀C和溶液D,故A中一定含有CaCO3、BaCl2和Na2SO4,则沉淀C应是BaSO4沉淀;白色固体混合物A中加入适量水,可得到溶液E和沉淀F,溶液E和溶液D,加入氯化铵溶液加热,生成气体G和溶液H,沉淀F与稀硝酸反应有气体生成,则气体G应是氨气,溶液E和溶液D中含有NaOH,根据“实验过程中所有可能发生的反应均恰好完全反应”,则混合物A中含有NaOH,不含MgCl2;故沉淀F为CaCO3和BaSO4,故现象二为:固体部分溶解(或有未溶解的固体,或上清液呈无色);
(1)沉淀C为硫酸钡,化学式为BaSO4,气体G为氨气,化学式为NH3。
(2)上图中现象二为固体部分溶解(或有未溶解的固体,或上清液呈无色)。
(3)A中含有BaCl2、Na2SO4、NaOH、CaCO3,加入稀盐酸恰好完全反应后,所得溶液D为氯化钠、氯化钙、氢氧化钠的混合溶液,故溶液D中肯定大量存在的阴离子是![]() 。
。
(4)步骤②中,BaCl2、Na2SO4、NaOH、CaCO3加入水,BaCl2与Na2SO4反应生成硫酸钡沉淀和氯化钠,反应的化学方程式为![]() 。
。
(5)步骤③中可能发生反应为氯化铵与氢氧化钠在加热条件下反应生成氯化钠、水和氨气(或氯化铵与氢氧化钙在加热条件下反应生成氯化钙、水和氨气),反应的化学方程式为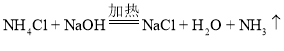 (或
(或 )。
)。
(6)由上述信息可推知,固体混合物A中一定不存在的物质是MgCl2,理由是:由图可知,步骤③中产生了NH3↑,说明溶液E和固体A中都存在NaOH,若固体A中含有MgCl2,它们会在步骤②中反应生成Mg(OH)2↓,则溶液E中将无OH-,导致步骤③中不会产生NH3↑,这与图中信息不符所以固体A中一定没有MgCl2(其他合理答案酌情给分)。

【题目】同学对酒精灯内、外焰温度高低进行如下探究。
实验一:将一根细木条迅速水平放入酒精灯火焰中,1~2s后取出,观察到位于外焰部分的木条炭化明显。
(1)由上述现象得出结论:内焰温度比外焰温度_____。(填“高”或“低”)
实验二:同学利用高温传感器测得酒精灯各层火焰平均温度如下表。
火焰层 | 焰心 | 内焰 | 外焰 |
平均温度/℃ | 432 | 666 | 520 |
(2)由上表得出结论:_____(填“焰心”、“内焰”或“外焰”)温度最高。
(提出问题)为什么实验一和实验二的结论不一致?
(查阅资料)①实验一中木条炭化是木条不完全燃烧的结果。
②锌的熔点为419.5℃,化学性质活泼,常温下在空气中表面能生成致密薄膜,可阻止其内部进一步氧化。
(猜想与假设)木条被灼烧部位的温度和氧气含量都会影响木条的炭化程度。
(设计实验)为了验证实验一和实验二哪个结论更准确,同学们设计了如外焰如图所示的实验。按图1将U型锌丝上下两端同时插入内、外焰中加热。图2是加热后锌丝两端向下弯折的情况。
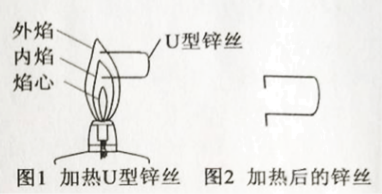
(现象与结论)
实验现象 | 结论 |
(3)U型锌丝_____(填“上”或“下”)端先发生弯折 | 实验二的结论正确 |
(反思与评价)
(4)U型锌丝加热之前_____(填“应该”或“不应该”)用砂纸打磨。理由是_____。
(5)铝的熔点是660℃,如果用U型铝丝替代锌丝进行实验,请你预测加热后铝丝的变化情况_____。(用文字表述或仿照图2画图表示均可)
(6)请阐述用U型锌丝替代细木条的优点_____(答2条)。
【题目】除去下列物质中的少量杂质,所用试剂和操作方法均正确的是( )
选项 | 物质 | 所用试剂和操作方法 |
A | N2(O2) | 通过灼热的木炭 |
B | KC1固体(MnO2) | 加入适量水溶解,过滤,洗涤,干燥 |
C | NaNO3溶液(CuSO4) | 加入过量Ba(NO3)2溶液,过滤 |
D | Cu(NO3)2溶液(HNO3) | 加入过量氧化铜粉末,过滤 |
A.AB.BC.CD.D