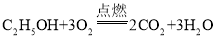题目内容
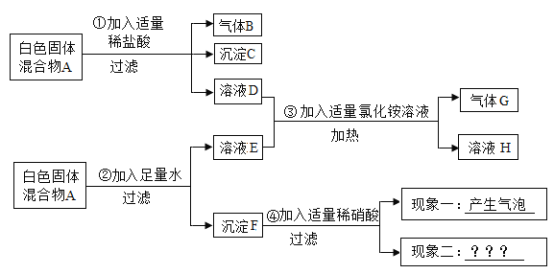
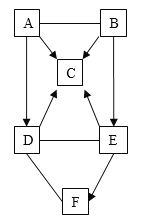
【题目】![]() 是初中化学常见的六种物质,其中只有D中不含有氧元素,B是一种钾盐,C、F属于相同类别的物质,且C的固体常用于人工降雨。图中“一”表示相连的两种物质之间可以发生反应,“
是初中化学常见的六种物质,其中只有D中不含有氧元素,B是一种钾盐,C、F属于相同类别的物质,且C的固体常用于人工降雨。图中“一”表示相连的两种物质之间可以发生反应,“![]() ”表示物质间存在着相应的转化关系
”表示物质间存在着相应的转化关系![]() 部分反应物、生成物及反应条件已略去
部分反应物、生成物及反应条件已略去![]() 。请回答下列问题:
。请回答下列问题:
(1)C的化学式是______,
(2)DF的基本反应类型是______,
(3)写出![]() 的化学方程式______,
的化学方程式______,
(4)写出![]() 的化学方程式______。
的化学方程式______。
【答案】![]() 复分解反应
复分解反应 ![]()
![]()
【解析】
A~F是初中化学常见的六种物质,C的固体常用于人工降雨,所以C为二氧化碳,B是一种钾盐可以生成二氧化碳,所以B为碳酸钾,B可以生成E,E也可以生成二氧化碳,E可以为碳酸钙,其中只有D中不含有氧元素,D可以与E反应也可以生成C,所以D为盐酸,A可以与B反应,同时又可以生成C和D,所以A为硫酸,C、F属于相同类别的物质,且F可由E制得,所以F为氧化钙,经过验证,推导正确。
(1)由分析可知,C为二氧化碳,故填:![]() 。
。
(2)D为盐酸,F为氧化钙,酸与金属氧化物的反应属于复分解反应,故填:复分解反应。
(3)B为碳酸钾,C为二氧化碳,碳酸钾与盐酸反应生成氯化钾、水和二氧化碳,化学方程式为:![]() ,故填:
,故填:![]() 。
。
(4)A为硫酸,D为盐酸,氯化钡与硫酸反应可以生成硫酸钡和盐酸,化学方程式为:![]() ,故填:
,故填: ![]() 。
。

【题目】取20g碳酸钠和碳酸氢钠的固体混合物,加热至不再产生气体2NaHCO3![]() Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
时间 | 0分钟 | 1分钟 | 2分钟 | 3分钟 |
仪器和浓硫酸的质量总和(g) | 150 | 150.9 | 151.8 | 151.8 |
(1)当完全反应后,生成水的质量为_____g。
(2)计算混合物中碳酸氢钠的质量分数________。(要求写出计算过程)
(3)将上述混合物完全分解后的固体溶解于186.2g 水中,待固体完全溶解后所得溶液中溶质的质量分数为_____。
【题目】为测定某氧化铜和铜的固体混合物中氧化铜的质量分数,小勇同学取20g固体混合物置于烧杯中,将100g稀硫酸分为四等份依次加入其中进行实验,测得数据如下:
次序 | ① | ② | ③ | ④ |
加入稀硫酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 16 | a | 10 | 10 |
回答下列问题:
(1)原固体混合物中,氧化铜的质量分数为_____。
(2)上表中,a的值为_____。
(3)计算该实验所用稀硫酸中溶质的质量分数。_____(写出计算过程,结果精确到0.1%)