题目内容
【题目】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。已知:Sn+SnCl4=2SnCl2。
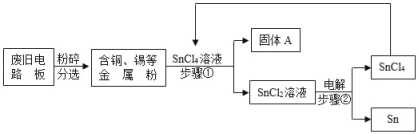
(1)步骤①的操作是_____。
(2)固体A中一定含有的金属元素是_____(填元素符号)。
(3)写出步骤②发生反应的化学方程式_____,该流程中可以循环利用的物质是_____。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是_____(回答一点即可)。
【答案】过滤 Cu 2SnCl2![]() SnCl4+Sn SnCl4 保护环境或节约金属资源(合理即可)
SnCl4+Sn SnCl4 保护环境或节约金属资源(合理即可)
【解析】
(1)根据过滤可以将不溶性固体从溶液中分离出来,所以步骤①的操作为过滤;
(2)铜的金属活动性比锡的弱,因此加入铜不能与SnCl4反应,所以固体A中一定含有的金属元素是Cu;
(3)步骤②中SnCl2通电分解生成SnCl4和Sn,发生反应的化学方程式为2SnCl2 ![]() SnCl4+Sn;根据反应可知循环利用的物质是 SnCl4;
SnCl4+Sn;根据反应可知循环利用的物质是 SnCl4;
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是保护环境;

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目