题目内容
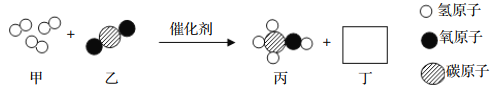
【题目】某小组同学利用传感器对碳酸氢钠、碳酸钠的某些性质进行以下探究。
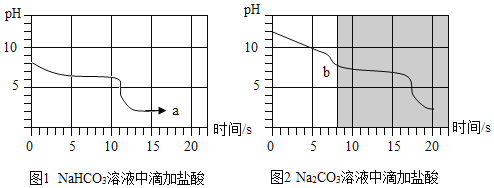
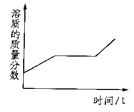
25℃时,向等体积、含有等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入相同浓度的盐酸,利用pH传感器测得pH变化与时间的关系如图1、图2所示,将图1、图2的阴影部分进行叠加,发现两者基本重合。
回答下列问题:
(1)等体积、含有等碳原子数的碳酸氢钠和碳酸钠溶液均呈碱性,两种溶液中碱性较强的是_____。
(2)a点的溶质为_____,b点前发生反应的化学方程式为_____。
(3)含有等碳原子数的碳酸氢钠和碳酸钠溶液,加入足量的盐酸,产生二氧化碳的质量_____。
A 碳酸氢钠多 B 碳酸钠多 C 两者一样多 D 不能确定哪个多
【答案】碳酸钠(或Na2CO3) NaCl、HCl Na2CO3+HCl=NaCl+NaHCO3 C
【解析】
(1)碱性溶液pH大于7,显碱性溶液pH越高,碱性越强,两种溶液中碱性较强的是碳酸钠(或Na2CO3);
(2)实验中,a点的溶质有碳酸氢钠和盐酸反应生成的氯化钠和过量的盐酸中的氯化氢;b点前,碳酸钠和稀盐酸反应生成氯化钠、碳酸氢钠,发生反应的化学方程式为:Na2CO3+HCl=NaCl+NaHCO3;
(3)由于是向含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别加入足量的盐酸,根据碳原子守恒,最终生成二氧化碳的量相等。

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目