题目内容
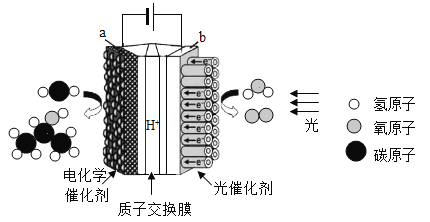
【题目】新能源汽车越来越受到人们的青睐,某新能源汽车定位系统微电脑控制器应用了一种新型无机非金属材料氮化铝(AlN)。某AlN样品中含有不与NaOH溶液反应的杂质,为测定AlN的含量,设计如下实验方案。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
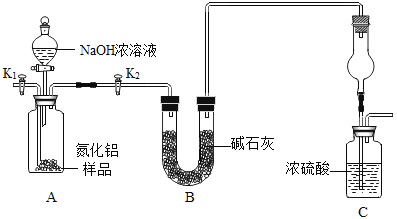
方案:取一定量的样品,用如图所示装置测定样品中AlN的纯度(夹持装置已略去)。
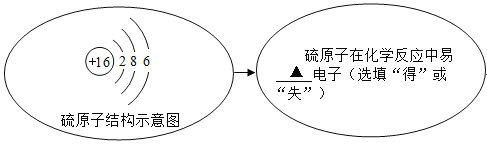
(1)AlN中氮元素化合价_____。
(2)图中C装置中球形干燥管的作用_____。
(3)实验操作:
①组装好实验装置,首先_____,再加入实验药品;
②接下来的实验操作是_____,打开分液漏斗活塞,缓慢滴加NaOH浓溶液至不再产生气体为止,缓慢滴加的原因_____。
③打开K1,向装置内缓慢通入氮气一段时间。通入氮气的目的是_____。
④反应前整个C装置的质量为200.2克,反应后整个C裝置的质量为203.6克,样品的质量为9.0克,计算样品中AlN的质量分数_____(写下计算过程,保留到0.1%)。
【答案】-3 防止倒吸 检查装置气密性 关闭K1,打开K2 使反应更充分,让产生的氨气被浓硫酸充分吸收 使滞留在装置内的氨气进入C中被浓硫酸充分吸收 91.1%
【解析】
(1)AlN中Al元素的化合价为+3,设N的化合价为x,则(+3)+x=0,解得x=-3,所以AlN中N的化合价为-3;
(2)由于氨气与硫酸发生反应,装置内压强变小,易发生倒吸,图中C装置中球形干燥管的作用是防倒吸;
(3)①该实验中有气体参与,因此组装好仪器后,应该检查装置的气密性,然后再装入药品;
②接下来的操作是为了使反应发生,并使产生的气体通过B,则需要关闭K1,打开K2,打开分液漏斗活塞,缓慢滴加NaOH浓溶液至不再产生气体为止,缓慢滴加的原因是使反应更充分,让产生的氨气被浓硫酸充分吸收;
③打开K1,向装置内缓慢通入氮气一段时间。通入氮气的目的是使滞留在装置内的氨气进入C中被浓硫酸充分吸收;
④反应前整个C装置的质量为200.2克,反应后整个C裝置的质量为203.6克,增加了3.4g,说明产生了3.4g氨气。
设样品中氮化铝的质量为y
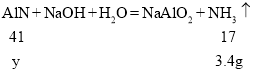
![]()
y=8.2g
则样品中AlN的质量分数为:![]() 。
。

【题目】设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的是( )
编号 | ① | ② | ③ | ④ |
实验设计 |
|
|
|
|
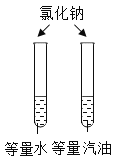
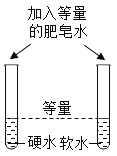
实验目的 | 探究同种物质在不同溶剂中的溶解性 | 区分硬水和软水 | 探究铁生锈的条件 | 研究二氧化锰的催化作用 |
A.①B.②C.③D.④