题目内容
【题目】氯碱工业是指用电解饱和NaCl溶液的方法来抽取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,电解饱和NaCl溶液的化学方程式为: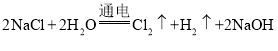 ,请计算:
,请计算:
(1)烧碱中三种元素的质量比m(Na):m(O): m(H)= 。
(2)用这种方法制备40t烧碱,需要NaCl的质量为 。
(3)若用25%的NaCl溶液按照上述方法电解并制取40t烧碱,完全电解后所得溶液的质量分数。( 假设生成的烧碱全溶,计算时若除不尽保留到1%) .
【答案】(1)23:16:1 (2)58.5t (32)20.3%
【解析】
解:(1)(1)烧碱中三种元素的质量比m(Na):m(O): m(H)=23:16:1;
(2)用这种方法制备40t烧碱,需要NaCl的质量为x,产生氢气的质量为y,产生氯气的质量为z。
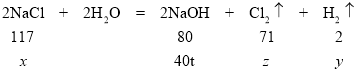
![]() x=58.5t
x=58.5t
![]() z=35.5t
z=35.5t
![]() y=1t
y=1t
用这种方法制备40t烧碱,需要NaCl的质量为58.5t;
(3)需要用25%的NaCl溶液质量=![]() ,
,
完全电解后所得溶液的质量分数=![]() 。
。

【题目】(1)某同学用市售浓盐酸(溶质质量分数为37%,密度为1.18gmL-1)配制800g溶质质量分数为10%的稀盐酸。通过计算可知需要浓盐酸 mL,水(密度lgmL-1) mL(上述两空答案都精确到0.1mL)
(2) 长期使用的热水锅炉会产生水垢。水垢主要成分是碳酸钙和氢氧化镁。某兴趣小组为了测定水垢中CaCO3的含量,将6g水垢粉碎后放在烧杯中,然后向其中加入40g某浓度的稀盐酸,使之充分反应(水垢中除碳酸钙和氢氧化镁外都不与稀盐酸反应)。实验数据记录如下:
反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
烧杯内所盛物质的总质量/g | 46.0 | 45.2 | 44.8 | 45.1 | 44.1 | 43.9 | 43.8 | 43.8 |
①表中有一数据是不合理的,该数据的测得时间是第 min。
②根据以上数据计算水垢中CaCO3的质量分数(计算结果精确至 0.1%)。