题目内容
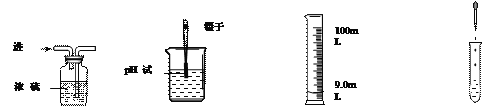
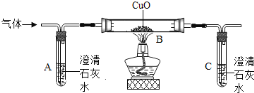
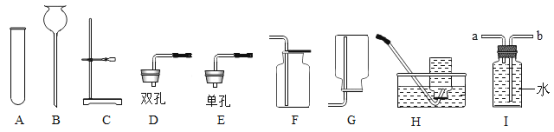
【题目】实验室制取气体的常用装置如下图所示。
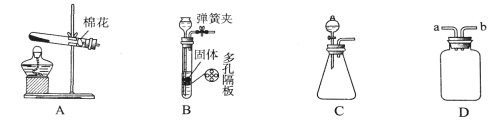
(1)写出用装置A来制取O2的化学方程式_______________。
(2)装置B或C均可作制取H2和CO2的发生装置,装置B的优点是能控制反应的发生和停止,请简述使装置B中反应停止的原理____________。
(3)若用装置D收集一瓶H2,气体从b口进入,请把装置D补画完整_______(只画导气管)。
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑ 关闭弹簧夹,试管内压强增大,液体药品被压入多孔塑料板以下,固液分离,反应停止
K2MnO4+MnO2+O2↑ 关闭弹簧夹,试管内压强增大,液体药品被压入多孔塑料板以下,固液分离,反应停止 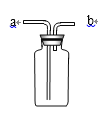
【解析】
(1)A装置有酒精灯,试管口有一团棉花,适用于加热高锰酸钾制取氧气,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;故填:2KMnO4
K2MnO4+MnO2+O2↑;故填:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(2)B装置中反应停止的原理是:关闭弹簧夹,试管内压强增大,液体药品被压入多孔塑料板以下,固液分离,反应停止;故填:关闭弹簧夹,试管内压强增大,液体药品被压入多孔塑料板以下,固液分离,反应停止;
(3)氢气的密度比空气密度小,要短进长出采用向下排空气法收集;
故填: 。
。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案【题目】硫酸锌可作为食品锌强化剂的原料.工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3 、MgO、CaO等,生产工艺流程示意如下:

[相关资料]不溶性碱受热分解后生成对应的氧化物。
(1)将菱锌矿研磨成粉的目的是 _______
(2)完成“氧化除铁”步骤中反应的化学方程式:2Fe(OH)2+Ca(ClO)2+2H2O=2____+CaCl2,这个反应中有______种元素的化合价发生了变化。
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,化学式是FeO(OH),组成元素Fe、O、H的质量比是________;
(4)根据下表数据,调节“滤液2”的pH范围为 _________;
Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
开始沉淀的pH | 10.4 | 6.4 | - | - |
沉淀完全的pH | 12.4 | 8.0 | - | - |
开始溶解的pH | - | 10.5 | - | - |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是 _______(选填序号).
a大理石粉 b石灰乳 c纯碱溶液 d烧碱溶液
(6)“滤液4”之后的操作依次为 :蒸发浓缩、________、过滤,洗涤,干燥.
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于 _______.