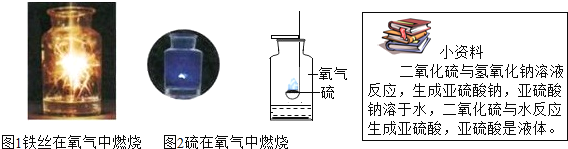
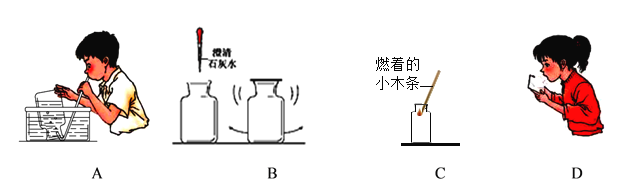
题目内容
【题目】 A和C都是常见的黑色粉末,A、B、E中含有同一元素,红色固体 D能发生如下转化:

(1)则A是_____,C是_____,D是_____。
(2)写出下列反应的化学方程式:A+B→E:_____;C+E→D+B:_____。该反应属于_____。
【答案】碳 氧化铜 铜 CO2+C![]() 2CO CuO+CO
2CO CuO+CO![]() Cu+CO2 氧化﹣还原反应
Cu+CO2 氧化﹣还原反应
【解析】
A和C都是常见的黑色粉末,A、B、E中含有同一元素,结合图中各物质的转化关系可知,A为碳、B为二氧化碳,E为一氧化碳,碳完全燃烧生成二氧化碳,二氧化碳和碳高温条件下生成一氧化碳;红色固体 D为铜,铜和氧气在加热条件下生成氧化铜,氧化铜和一氧化碳在高温条件下反应生成铜和二氧化碳。
(1)则A是碳,C是氧化铜,D是铜;
(2)碳和二氧化碳反应生成一氧化碳,反应的化学方程式:CO2+C![]() 2CO;一氧化碳和碳高温条件下生成一氧化碳的方程式为:CuO+CO
2CO;一氧化碳和碳高温条件下生成一氧化碳的方程式为:CuO+CO![]() Cu+CO2,一氧化碳得氧成为二氧化碳,发生了氧化反应,氧化铜失氧成为铜,发生了还原反应,该反应属于氧化﹣还原反应。
Cu+CO2,一氧化碳得氧成为二氧化碳,发生了氧化反应,氧化铜失氧成为铜,发生了还原反应,该反应属于氧化﹣还原反应。

 小学课时特训系列答案
小学课时特训系列答案【题目】小明、小芳二位同学为探究稀硫酸的化学性质,做了如下实验:
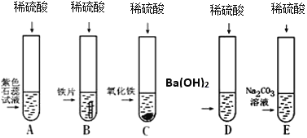
(1)试管A中的现象是____,反应后试管B中一定有的阳离子是____(写离子符号)。
(2)试管C中反应的化学方程式为_____。
(3)试管D中反应的化学方程式为____。
小芳同学把反应后D、E试管中的废液倒入一个洁净的烧杯中,过滤,得到白色沉淀和无色滤液,她决定对白色沉淀的成分进行探究。
(查阅资料)硫酸钡不溶于酸。
(作出猜想)I.BaSO4;II.BaCO3;III._____。
(拓展与反思)猜想II不成立,原因是_____。
(实验方案)
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若沉淀全部不溶解;猜想Ⅰ成立; ②若____,且有气泡产生,猜想III成立,其化学反应方程式为____。 |
【题目】在一定条件下,NH3可以燃烧,且该反应能放出大量的热。下表是测定的部分数据
纯净物 | NH3 | O2 | H2O | X |
反应前质量/g | 1.7 | 3 | 0 | 0 |
反应后质量/g | 0 | 0.6 | 2.7 | 待测 |
根据数据可以判断下列选项正确的是: ( )
A. 反应后X的质量是2gB. X是由氮元素组成
C. X是由氮元素和氧元素组成D. X是由氮元素.氢元素.氧元素组成