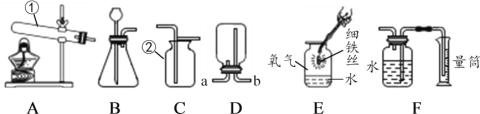
题目内容
【题目】某化工厂排出的废水中含有硝酸银和硝酸铜。为了测定该废水的组成,取1000g的废水加入锌粉,所得溶液的质量与加入锌粉质量关系如图,请计算:
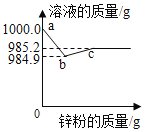
(1)该溶液中硝酸银溶液的质量分数为_____(结果精确到0.1%,下同)。
(2)反应完全后所得溶液的溶质质量分数为_____。
【答案】3.4% 7.7%
【解析】
锌粉和硝酸银先反应生成硝酸锌和银,完全反应后,多余的锌和硝酸铜反应生成铜和硝酸锌。
设溶液中硝酸银溶液的质量分数为x,生成的硝酸锌的质量为y

![]()
x=3.4%
y=18.9g
结合曲线上升阶段的溶液质量差是因为锌和硝酸铜所致,
设生成的硝酸锌的质量为z
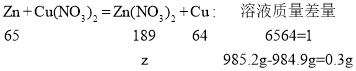
![]()
z=56.7g
反应完全后所得溶液的溶质质量分数为![]() ×100%≈7.7%。
×100%≈7.7%。
答:该溶液中硝酸银溶液的质量分数为3.4%,反应完全后所得溶液的溶质质量分数为7.7%。

 阅读快车系列答案
阅读快车系列答案【题目】水与自然界中矿石长期接触,常含Ca(HCO3)2、Mg(HCO3)2等物质,导致钙离子、镁离子含量较多,称之为硬水。生活中,水的硬度过高会造成一定危害。长期使用硬水烧水的热水壶,内部会形成一层水垢,其主要成分为碳酸钙和氢氧化镁,说明加热煮沸可使这类硬水成为软水。其原理的流程如下、题(气体产物已略去):
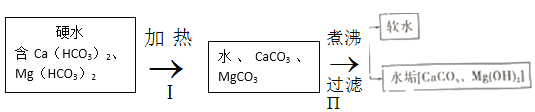
回答下列问题:
(1)反应Ⅰ属于四大基本反应类型中的________反应;反应Ⅱ除产生水垢外,还有一种气体产物为________;如果当地硬水中CaSO4含量较多,则水垢中还常含有少量CaSO4,CaSO4析出的原因是________。
(2)向200g水垢中加入400g过量的稀盐酸,充分反应,测得3分钟内混合物质量的变化(不考虑水与HCl的挥发)如下表所示:
时间/s(秒) | 0 | 30 | 60 | 90 | 120 | 180 |
混合物的质量/g | 600 | 574 | 554 | 547.2 | 547.2 | 547.2 |
①观察到的现象是____
②计算水垢中碳酸钙的质量分数____,写出必要的计算过程。
【题目】有镁和氯化镁固体混合物,取一定量的该混合物放入烧杯中,然后取稀盐酸200g,平均分五次加入其中,充分振荡,实验所得数据如下表:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的质量/g | 40 | 40 | 40 | 40 | 40 |
生成气体的总质量/g | 0.16 | m | 0.48 | 0.5 | 0.5 |
(1)表中m的值为_____。
(2)所用稀盐酸的溶质质量分数为多少?____