题目内容
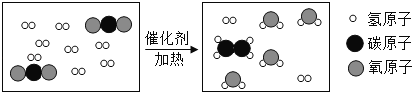
【题目】化学反应过程中有元素化合价变化的化学反应叫做氧化还原反应;反应中元素化合价的变化,是电子转移的外观表现。例如在氢气还原氧化铜的反应中,氢气是还原剂,氧化铜是氧化剂,铜是还原产物,水是氧化产物,如图所示:
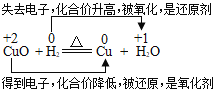
(1)初中化学基本反应类型中,化学反应一定不属于氧化还原反应的是_____。
(2)进一步定量分析氢气还原氧化铜的反应中,氧化剂得电子总数_____(填“>”、“=”或“<”)还原剂失电子总数。
(3)铜能与一定浓度硝酸发生如下反应:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O,该反应中,还原剂是____,还原产物有____。如果生成的NO和NO2的分子个数比为1:1,写出该反应的化学方程式:_____。
【答案】复分解反应 = 铜 一氧化氮和二氧化氮 2Cu+6HNO3=2Cu(NO3)2+NO↑+NO2↑+3H2O
【解析】
四大基本反应类型:化合反应,分解反应,置换反应和复分解反应。
(1)化学反应过程中有元素化合价变化的化学反应叫做氧化还原反应,而复分解反应没有单质参与生成一定不是氧化还原反应。
(2)由氢气还原氧化铁的反应可知,氧化剂得电子总数等于还原剂失电子总数,故氧化剂得电子总=还原剂失电子总数。
(3)在反应中,铜失去电子被氧化,是还原剂;硝酸中的部分氮原子得到电子被还原,是氧化剂;一氧化氮和二氧化氮是还原产物;如果生成的NO和NO2的分子个数比为![]() ,则化学方程式为
,则化学方程式为![]() 。
。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案【题目】以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | |
Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 | 48.5 | 46.0 |
NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 |
A. 40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B. 60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C. 30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D. 20℃的饱和Na2CO3溶液中通足量CO2,生成的NaHCO3会部分析出