题目内容
【题目】硝苯地平控释片是一种治疗高血压药物,其主要成份为硝苯地平(C17H18N2O6)。请回答下列问题:

(1)“硝苯地平控释片”属混合物__________(填 “纯净物”或“混合物”)。
(2)“硝苯地平”由_______种元素组成, C、H、N、O的质量比为___________。
从“硝苯地平控释片”的贮藏方法中可判断“硝苯地平”可能的化学性质是________。
【答案】混合物 4 102:9:14:48 见光(受热)易分解
【解析】
(1)硝苯地平控释片主要成份为硝苯地平,说明硝苯地平控释片属于混合物;
(2)根据硝苯地平化学式(C17H18N2O6)可知其由碳、氢、氮、氧四种元素组成,碳、氢、氮、氧四种元素的质量比=(12×17):(1×18):(14×2):(16×6)=204:18:28:96=102:9:14:48;
(3)根据“遮光,30'℃以下密封保存,从铝塑振中瓢出后应立即服用”可知见光(受热)易分解。

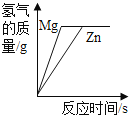
【题目】在校园科技节上,为测出鸡蛋壳(主要成分是碳酸钙)中碳酸钙的质量分数,某同学称取已洗净、晾干、研成粉末的鸡蛋壳10g置于烧杯中,将烧杯放在电子天平上,往烧杯中平均分5次加入50g的稀盐酸,测得实验数据如表:
实验次数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸质量/g | 10.0 | 20.0 | 30.0 | 40.0 | 50.0 |
剩余物质质量/g | 19.0 | 28.0 | 37.0 | 46.7 | 56.7 |
(1)第__________ 次实验时鸡蛋壳已经完全反应。
(2)假定鸡蛋壳中的其它物质不会与稀盐酸反应,试计算出该鸡蛋壳中碳酸钙的质量分数________。(写出具体计算过程)
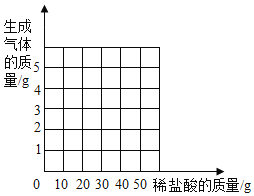
(3)请在图中画出加入稀盐酸的质量与生成气体的质量的变化关系________(标注必要的数值)
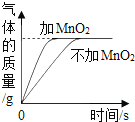
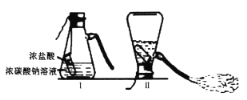
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究。
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质可能是NaCl、Na2CO3和HCl。
猜想2:废液中的溶质只有NaCl。
猜想3:废液中的溶质是NaCl和HCl。
猜想4:废液中的溶质是_________。
(讨论与交流)
小明认为猜想1无需验证就知道是错误的,他的理由是_______。(请用化学方程式说明)
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现酚酞溶液不变色,于是小亮认为猜想3正确。他的结论错误理由是__________。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
__________ | ______ | 猜想3正确 |
(2)验证猜想4,可选用的的试剂有___________。
A.酚酞溶液 B.氢氧化钾溶液 C.稀硫酸 D.氯化钡溶液。
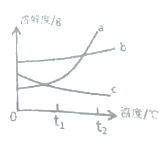
【题目】t1℃时,将甲、乙、丙三种固体各20克,分别加入盛有50克水的烧杯中,充分溶解后的情况如下表
物质 | 甲 | 乙 | 丙 |
未溶解的固体/g | 5.4 | 0 | 2 |
(1)一定是饱和溶液的是_______,t1℃时丙的溶解度为_______。
(2)图中表示固体甲的曲线是________。
(3)t1℃时,甲乙丙的溶解度大小关系为_______。
(4)t2℃时,取等质量的甲乙丙的饱和溶液,分别恒温蒸发等质量的水,析出溶质质量的大小关系为______(用甲乙丙表示)