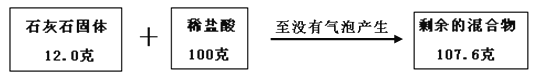
题目内容
【题目】下列实验原理与化学反应方程式的书写都正确的是()
A. 用熟石灰和盐酸反应:CaO+2HCI=CaCl2+H2O
B. 洗去试管壁上附着的铜:Cu+H2SO4=CuS04+H2↑
C. 铁丝在氧气中燃烧:4Fe+302![]() 2Fe203
2Fe203
D. 用氢氧化钠吸收二氧化硫:2NaOH+SO2=Na2S03+H20
【答案】D
【解析】
A、熟石灰学名氢氧化钙,化学式为Ca(OH)2,与盐酸反应生成氯化钙和水,化学方程式为Ca(OH)2+2HCI=CaCl2+2H2O,选项错误;B、根据金属活动性顺序可知,铜无法与稀酸反应,选项错误;C、铁丝在纯氧中燃烧生成黑色的四氧化三铁,化学式为Fe3O4,化学方程式为3Fe+2O2![]() Fe3O4,选项错误;D、氢氧化钠和二氧化硫反应生成亚硫酸钠和水,选项正确。故本题选D。
Fe3O4,选项错误;D、氢氧化钠和二氧化硫反应生成亚硫酸钠和水,选项正确。故本题选D。

 寒假乐园北京教育出版社系列答案
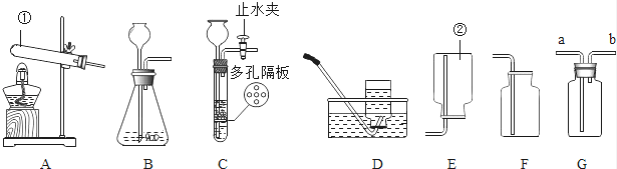
寒假乐园北京教育出版社系列答案【题目】实验设计时化学实验的重要环节,请根据下列实验要求回答相关问题:
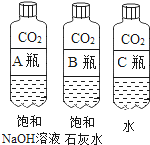
(活动与探究一)用对比实验方法探究二氧化碳的性质.
实验一 | 实验二 |
|
|
(1)实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为________;对比A瓶与________(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
(2)实验二观察到C装置中发生的现象是________,结论是________(用化学方程式表示).
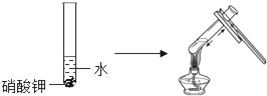
(活动与探究二)用变量控制方法探究影响物质溶解性的因素.
实验三 | 实验四 |
|
|
(3)实验三目的是探究________对硝酸钾溶解性的影响;实验四是探究溶剂种类对物质溶解性的影响,该实验中需要控制的变量是温度和________.
(活动与探究三)定量测定空气中氧气的含量.
实验五
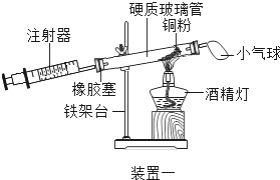

(4)实验五中,反应的原理为________(用化学方程式表示);装置一比装置二更合理,理由是________;
(5)根据下表提供的实验数据,完成下表:
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
30mL | 20mL | 12mL | ________ |
定量实验操作中易产生误差,如果反应前气球中存在气体(其量小于注射器内的空气),而实验后冷却至室温,将气球内的气体全部挤出读数,导致实验测得结果________(填“偏小”、“偏大”或“无影响”).