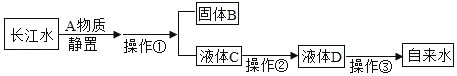
题目内容
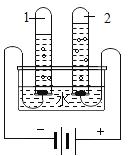
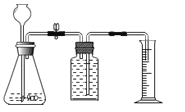
【题目】如下图为电解水的实验装置图,下列说法正确的是( )
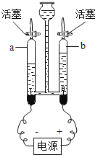
A.在水中加入少量硫酸钠以增强水的导电性
B.a管收集到的气体能使带火星的木条复燃
C.该实验中所得氢气和氧气的质量比约为2∶1
D.该实验可得到的结论:水中含氢分子和氧分子。
【答案】A
【解析】
电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2;电解水时在水中加入少量氢氧化钠、硫酸钠或稀硫酸以增强导电性。
A、在水中加入少量硫酸钠以增强导电性,故说法正确;
B、由电解水的装置可知,负极产生的气体较多是H2,氢气具有可燃性,不能使带火星的木条复燃,故说法错误;
C、电解水时,正极产生的是氧气,负极产生的是氢气,氢气和氧气的体积比约为2:1;故说法错误;
D、电解水生成了氢气和氧气,说明了水是由氢、氧两种元素组成的,故说法错误;
故选:A。

 高中必刷题系列答案
高中必刷题系列答案【题目】在化学实验课上,小组同学利用回收的二氧化锰来催化过氧化型制取氧气,但发现利用回收的二氧化锰作为催化剂反应速率很慢.查阅资料得知:催化剂在催化过程中催化剂的活性减弱或失去,这种现象叫做催化剂的中毒.为了探究影响二氧化锰催化能力降低的因素,在老师的指导下,小组同学进行如下实验:
(实验准备)
取三份质量均为1克的二氧化锰分别催化50毫升溶质质量分数为5%、15%、25%的过氧化氢溶液分解,试验后回收二氧化锰,并分别标为②、③、④;另取多次催化分解5%过氧化氢实验后回收的二氧化锰,标为⑤。
(实验步骤)
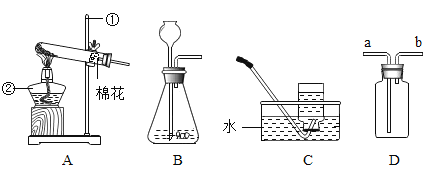
(1)连接仪器,检查装置气密性,检查该实验气体发生装置气密性的方法是_______。
(2)取未使用过的二氧化锰0.5克,标为①,加入锥形瓶中,再加入10毫升溶质质量分数为5%的过氧化氢溶液,记录收集20s时间气体的体积.
(3)再分别取②、③、④、⑤组二氧化锰各0.5克,重复上述实验。
(4)采取多次实验取平均值的方法,实验数据记录如下:
组别 | ① | ② | ③ | ④ | ⑤ |
收集气体体积/ml | 118 | 92 | 87 | 77 | 62 |
(回答下列问题)
①实验过程中量筒的作用是________
②实验中,除了通过比较收集相同时间内产生的气体体积,还可以通过比较_________来对比二氧化锰的催化效果。锥形瓶中残留的空气对测量结果_________(填“有”或“没有”)。
③请写出该实验反应的符号表达式__________
(5)由表中实验_______(填实验序号)数据可知,影响回收的二氧化锰催化效率下降的因素有二氧化锰的使用次数。由表中实验数据②、③、④数据可知,影响回收的二氧化锰催化效率下降的因素是______
(进一步探究)化学课本告诉我们,硫酸铜溶液也可以催化过氧化氢溶液的分解。小明通过前面的学习想知道硫酸铜是离子构成的,想知道硫酸铜溶液中的哪种粒子对过氧化氢溶液分解有催化作用产生了好奇。
(查阅资料)硫酸铜溶液中有铜离子、硫酸根离子和水分子;硫酸钠溶液中有钠离子,硫酸根离子和水分子。
(实验设计)
①根据所学知识判断水分子对过氧化氢分解_______(填“有”或“没有”)催化作用。
②提供药品:5%的过氧化氢溶液、硫酸铜溶液、硫酸钠溶液,仪器自选。请设计实验欲证明是铜离子对过氧化氢有催化作用____________(包括操作、现象、结论)。
【题目】用久置的镁条做实验时,需要用砂纸把表面的灰黑色打磨掉,直到露出光亮的银白色.实验小组同学对镁条表面“灰黑色外衣”的成分进行如下探究.
【提出问题】镁条表面“灰黑色外衣”的成分是什么?
【猜想与假设】
Ⅰ.是镁与空气中的氧气反应生成的氧化镁.
Ⅱ.是镁与空气中的二氧化碳反应生成的黑色碳单质.
Ⅲ.根据铜锈的成分是碱式碳酸铜,推测镁条表面的“灰黑色外衣”是镁在潮湿的空气中生锈得到的碱式碳酸镁.
同学们经讨论,从颜色上否定了只含有氧化镁,因为氧化镁是 .
【查阅资料】
①碱式碳酸镁的性质有:受热可分解;常温下能与稀硫酸反应.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应,但与浓硫酸在加热条件下能反应并生成CO2、SO2和H2O.
同学们认为碳与浓硫酸反应生成三种产物的共同点是 (答出一点即可).
【进行实验】
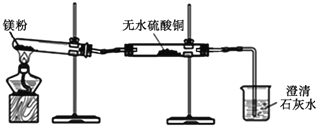
(1)同学们用久置的镁粉进行了如下实验.
实 验 装 置 |
|
实 验 现 象 | ①无水硫酸铜粉末逐渐由白色变为蓝色 ②澄清石灰水变浑浊 |
结 论 | 久置的镁粉中除镁元素外,还含有的元素是 久置的镁粉中含有碱式碳酸镁 |
(2)同学们发现,经加热一段时间后,试管中镁粉会突然“噗”地燃烧起来,出现红热,很快停止,并有黑色固体粘附在试管壁上.
①将试管取下,冷却后加入足量稀硫酸,大部分固体溶解,并有气泡出现,但黑色固体没有消失.请写出有气体生成的一个反应化学方程式 .
②将实验①试管中的混合物进行 (填操作名称),除去其中溶液,向黑色固体中加入浓硫酸,加热.黑色固体全部溶解,得澄清溶液并伴有刺激性气味的气体产生.
实验(2)说明,镁在CO2中可以燃烧,生成了碳单质.
【实验结论】
综合上述实验现象,实验小组认为镁条表面“灰黑色外衣”中含有碳和碱式碳酸镁.
【反思与评价】
有的同学提出,实验(2)不足以证明镁条表面“灰黑色外衣”中含有碳,他的理由是 .