题目内容
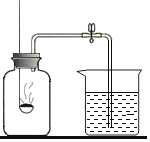
【题目】某兴趣小组用74g氯酸钾样品(杂质不参加反应且不含氧元素)和wg二氧化锰混合共热,完全反应后、冷却制得19.2g氧气,剩余固体72.8g,请计算:
(1)二氧化锰的质量______
(2)受热分解的氯酸钾的质量______
(3)氯酸钾样品中氧元素的质量分数(计算结果精确到0.1%。)______
【答案】18g 49g 25.9%
【解析】
氯酸钾受热时,在二氧化锰的催化作用下,分解生成氯化钾和氧气。
(1)根据质量守恒定律,反应前反应物的质量等于反应后生成物的质量,二氧化锰的质量为![]() 。
。
(2)设受热分解的氯酸钾的质量为x
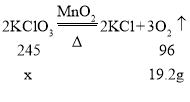
![]()
![]()
故受热分解的氯酸钾的质量为49g。
(3)氯酸钾样品中氧元素的质量为![]()
氯酸钾样品中氧元素的质量分数为![]()

练习册系列答案
相关题目
【题目】实验室现有硫酸铜和硫酸钠的固体混合物样品,小明同学想测定样品中硫酸铜的质量分数。先称取该混合物样品25g,完全溶于水中,然后取用了一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
次数/物质的质量 | 1 | 2 | 3 | 4 |
加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
生成沉淀的质量/g | 4.9 | x | 14.7 | 14.7 |
(1)表中X的数值为________________;
(2)计算原固体混合物样品中硫酸铜的质量分数为___________?
(3)上述实验中所用到的氢氧化钠溶液,是小海同学利用实验室中已有的80g溶质质量分数为40%的氢氧化钠溶液配置的,计算需加入______克水(只写计算结果),才能配成实验中所需溶质质量分数的氢氧化钠溶液.