题目内容
【题目】Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,将100g稀硫酸分5次加入其中,使之充分反应.每次所用稀硫酸的质量及剩余物的总质量记录于右表:
加入稀硫酸的质量(g) | 充分反应后剩余物的总质量(g) | |
第1次 | 20 | 39.9 |
第2次 | 20 | 59.8 |
第3次 | 20 | 79.7 |
第4次 | 20 | 99.6 |
第5次 | 20 | 119.6 |
试回答下列问题:
(1)反应结束时产生氢气的质量为______________。
(2)黄铜样品中锌的质量分数是多少? (请写出计算过程)______
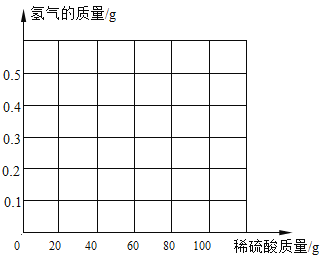
(3)请在下图画出氢气的产生曲线。______
【答案】0.4g 65% 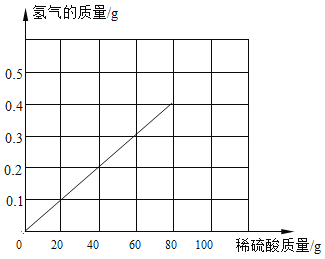
【解析】
(1)根据质量守恒定律可知:反应结束时产生氢气的质量为=10g+20g-119.6=0.4g;
(2)设生成0.4g的氢气需要锌的质量为x。
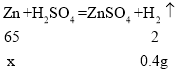
![]() x=13g;
x=13g;
黄铜样品中锌的质量分数=![]() ;
;
(3)根据表格中数据可知,恰好反应时,生成氢气0.4g,消耗稀硫酸80g,反应完后气体质量不再增加,可得氢气的产生曲线: 。
。

练习册系列答案
相关题目
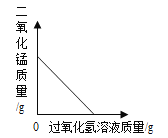
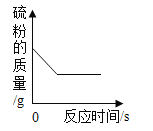
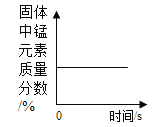
【题目】下列能正确反映相关变化关系的是()
|
|
|
|
A向一定质量的二氧化锰中加入过氧化氢溶液 | B一定量的硫粉与过量的氧气在密闭容器内点燃并充分反应 | C加热一定质量的高锰酸钾固体 | D等质量CaCO3分别与等体积等浓度的稀盐酸(足量)反应 |
A.AB.BC.CD.D