题目内容
【题目】下列属于分解反应的是
A. CO2 +H2O=H2CO3 B. CaCO3![]() CaO+CO2↑
CaO+CO2↑
C. Zn+H2SO4=ZnSO4+H2↑ D. 2NaOH+H2SO4=Na2SO4+2H2O
【答案】B
【解析】
A、CO2+H2O=H2CO3,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应,故选项错误;
B、CaCO3![]() CaO+CO2↑,该反应符合“一变多”的形式,符合分解反应的特征,属于分解反应,故选项正确;
CaO+CO2↑,该反应符合“一变多”的形式,符合分解反应的特征,属于分解反应,故选项正确;
C、Zn+H2SO4=ZnSO4+H2↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误;
D、2NaOH+H2SO4=Na2SO4+2H2O,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项错误。
故选B。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案【题目】某化学兴趣小组在探究物质燃烧条件时,做了如下实验:
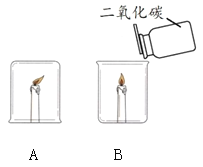
同学们发现两支蜡烛都熄灭了。
(提出问题)实验A中蜡烛熄灭的原因是什么?
(猜想与假设)
猜想1:烧杯内的氧气被耗尽,所以蜡烛熄灭。
猜想2:烧杯内的二氧化碳含量升高,所以蜡烛熄灭。
(进行实验)
实验I:点燃蜡烛,塞紧胶塞。待蜡烛熄灭后,用放大镜照射白磷。观察到白磷燃烧。
实验II:经检测,实验A中,蜡烛熄灭时,烧杯内二氧化碳的体积分数约为3%。在集气瓶中按照一定的体积比收集气体,分别放入燃烧的蜡烛和燃烧的红磷,实验记录如下:
V(O2):V(CO2) | 蜡烛 | 红磷 |
1:4 | 燃烧 | 燃烧 |
1:5 | 燃烧 | 燃烧 |
1:6 | 熄灭 | 燃烧 |
1:9 | 熄灭 | 燃烧 |
(解释与结论)
(1)实验B中蜡烛熄灭,体现二氧化碳的化学性质是_______。
(2)实验I的目的是_______。
(3)写出红磷燃烧的化学方程式_______。
(4)实验II证明猜想2错误,依据的实验现象是_______。
(5)结合实验I与实验II,得出的实验结论是_______。
(实验反思)
(6)通过此实验,同学们对物质燃烧的条件有了新的认识,如_______。