题目内容
【题目】根据下图所示仪器(装置)回答问题(省略夹持仪器)。
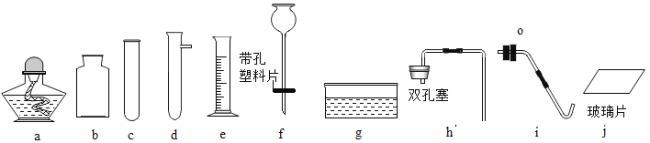
(1)仪器e的名称是__________。
(2)写出高锰酸钾制氧气的化学方程式:_________。制备并收集用于做铁丝燃烧实验的氧气,组装装置除需仪器a、c、i.j外,还需选用_______ (填标号),铁丝在氧气中燃烧的现象:_________。
(3)写出锌粒和稀硫酸制氢气的化学方程式:__________;欲使反应随时发生或终止,应选取仪器___ (填标号)组装发生装置。
【答案】量筒 2KMnO4![]() K2MnO4+MnO2+O2↑ b.g 剧烈燃烧,火星四射,生成黑色固体,放出大最的热 Zn+H2SO4=ZnSO4+H2↑ c、f、h
K2MnO4+MnO2+O2↑ b.g 剧烈燃烧,火星四射,生成黑色固体,放出大最的热 Zn+H2SO4=ZnSO4+H2↑ c、f、h
【解析】
(1)据图可知仪器e是量筒;
(2)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,化学方程式:2KMnO4![]() K2MnO4+MnO2+O2↑;制备并收集用于做铁丝燃烧实验的氧气,组装装置除需仪器a、c、i.j外,还需选用b、g;铁丝在氧气中燃烧的现象:剧烈燃烧,火星四射,生成黑色固体,放出大最的热;
K2MnO4+MnO2+O2↑;制备并收集用于做铁丝燃烧实验的氧气,组装装置除需仪器a、c、i.j外,还需选用b、g;铁丝在氧气中燃烧的现象:剧烈燃烧,火星四射,生成黑色固体,放出大最的热;
(3)锌和硫酸反应生成硫酸锌和氢气,化学方程式:Zn+H2SO4=ZnSO4+H2↑;欲使反应随时发生或终止,应选取仪器c、f、h组装发生装置。

【题目】铜是生活中常见的一种金属,在生活、生产中有广泛的应用。

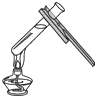
(1)如图为铜元素在元素周期表中的信息,铜元素的原子序数为___;
(2)铜离子(Cu2+)的核外电子数为____________;
(3)电气工业上常用铜作电缆的内芯,是利用铜具有良好的_____性;
(4)铜是一种不活泼的金属,但铜制品长期露置在潮湿空气中,表面变绿色,即生成了“铜绿”(化学式:Cu2(OH)2CO3)。
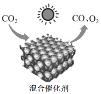
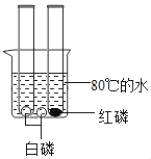
某同学根据铜绿的成分Cu2(OH)2CO3作出猜想:金属铜锈蚀的条件除有氧气和水外,还必须有二氧化碳。为证明“必须有二氧化碳”,需要进行如图所示实验中的_____(选填实验编号甲、乙、丙、丁)
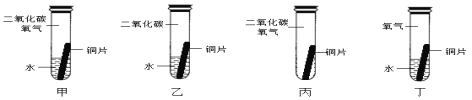
(5)某兴趣小组以锈蚀严重的废铜屑为原料(假设不含其他杂质)制取纯铜。如图是兴趣小组设计的两种回收铜的实验方案:
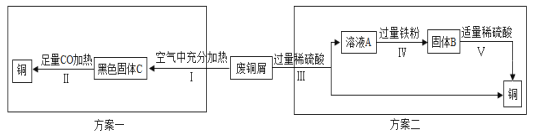
查阅资料:Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑
(分析评价)
①步骤Ⅲ、Ⅳ、Ⅴ都需要进行的实验操作是___________;
②步骤Ⅳ过程发生反应的化学方程式为__________________、_________________;
③同一份废铜屑分别通过上述两种方案最终得到的铜的质量:方案一_____(填“>”或“=”或“<”)方案二。以上两种方案中,方案二优越于方案一,理由是________(答一点)。
(拓展探究)在方案一中,小明和小丽分别取24克氧化铜,用CO还原,小明得到19.2克红色固体,小丽得到20.8克红色固体。为什么两人得到的红色固体质量不相等?
查阅资料:
Ⅰ.CO还原CuO时也可产生红色的氧化亚铜(Cu2O)
Ⅱ.Cu2O+H2SO4(稀)=Cu+CuSO4+H2O
他们分析推断:
④一致认为________(填“小明”或“小丽”)的产物中肯定含有Cu2O;
⑤用CO还原4克CuO得到红色固体a克,若红色固体为Cu和Cu2O的混合物,则a的取值范围为____________;
⑥可以用简单的实验验证红色固体中是否有Cu2O,请简述操作、现象及结论:_____。
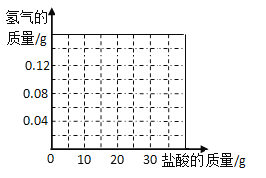
(6)我国约在南北朝时就开始冶炼黄铜。黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。为了测定某黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质),现将30g稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定本次生成氢气的质量,实验数据见表。试求:
第一次 | 第二次 | 第三次 | |
加入稀盐酸的质量(g) | 10 | 10 | 10 |
本次生成氢气的质量(g) | 0.04 | m | 0.02 |
①m=____________。
②此黄铜样品中铜的质量分数是多少_______?。
③稀盐酸的溶质质量分数是_______。
④在坐标系中画出生成氢气总质量与加入盐酸质量关系的图像。______