题目内容
(1)NH4Cl 在10℃时溶解度为33g,则10℃时NH4Cl 饱和溶液的溶质质量分数为______,200g饱和溶液含NH4Cl______g,含水______g.
(2)把一定质量的30%的某溶液加热蒸发10g水,冷却至20℃时,有2g晶体析出,此时溶液的质量分数为40%,则该物质在20℃时的溶解度为______g.
解:(1)NH4Cl在10℃时溶解度为33g,则10℃时NH4Cl饱和溶液的溶质质量分数为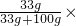 100%≈24.8%.
100%≈24.8%.
200g该温度下的饱和溶液含NH4Cl的质量为200g×24.8%=49.6g,含水的质量为200g-49.6g=150.4g.
(2)把一定质量的30%的某溶液加热蒸发10g水,冷却至20℃时,有2g晶体析出,所得溶液为20℃时的饱和溶液,饱和溶液中溶质的质量分数为40%,
设该物质在20℃时的溶解度为S,则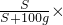 100%=40%,S=66.7g
100%=40%,S=66.7g
故答案为:(1)24.8%;49.6g;150.4g;(2)66.7.
分析:(1)根据饱和溶液的溶质质量分数=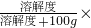 100%,进溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量即可求得水的质量,据此进行分析解答.
100%,进溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量即可求得水的质量,据此进行分析解答.
(2)将原溶液蒸发掉10g水后,冷却至20℃析出了晶体,根据饱和溶液的定义可知,该溶液为20℃时的饱和溶液,此时的溶质的质量分数即为该温度下的饱和溶液的质量分数,据此可计算出20℃时该物质的溶解度.
点评:本题难度不大,掌握饱和溶液的溶质质量分数的计算方法、溶质质量分数的有关计算等是正确解答本题的关键.
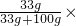 100%≈24.8%.
100%≈24.8%.200g该温度下的饱和溶液含NH4Cl的质量为200g×24.8%=49.6g,含水的质量为200g-49.6g=150.4g.
(2)把一定质量的30%的某溶液加热蒸发10g水,冷却至20℃时,有2g晶体析出,所得溶液为20℃时的饱和溶液,饱和溶液中溶质的质量分数为40%,
设该物质在20℃时的溶解度为S,则
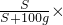 100%=40%,S=66.7g
100%=40%,S=66.7g故答案为:(1)24.8%;49.6g;150.4g;(2)66.7.
分析:(1)根据饱和溶液的溶质质量分数=
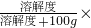 100%,进溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量即可求得水的质量,据此进行分析解答.
100%,进溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量即可求得水的质量,据此进行分析解答.(2)将原溶液蒸发掉10g水后,冷却至20℃析出了晶体,根据饱和溶液的定义可知,该溶液为20℃时的饱和溶液,此时的溶质的质量分数即为该温度下的饱和溶液的质量分数,据此可计算出20℃时该物质的溶解度.
点评:本题难度不大,掌握饱和溶液的溶质质量分数的计算方法、溶质质量分数的有关计算等是正确解答本题的关键.

练习册系列答案
相关题目
某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
【产品与原理】
该厂采用“侯氏制碱法”生产化工产品--纯碱(Na2CO3)和化肥NH4Cl.
生产原理是:将NH3和CO2通入饱和食盐水中得到NaHCO3和NH4Cl的混合物,反应为:
NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl;分离出NaHCO3,加热制得纯碱.
【生产流程】
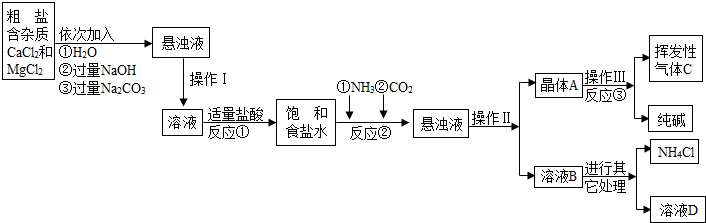
【相关资料】
(1)NH4Cl
NH3↑+HCl↑
(2)已知20℃时有关物质的溶解度如下
(气体指1体积水中能溶解的气体体积)
【问题讨论】:
(1)操作Ⅰ、Ⅱ、Ⅲ中,相同操作的名称为 .
(2)反应①中发生了两个反应,写出其中的一个化学方程式:
.
(3)反应③中得到纯碱的化学方程式为: .
(4)溶液B中的溶质有 (至少写出两种).
(5)上述生产流程中可循环使用的是 (填序号).
A.挥发性气体C; B.溶液D; C.氢氧化镁;D.化肥NH4Cl
【组成确定】
(1)称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.
由上述实验可确定纯碱样品含有杂质 (写化学式).
【含量测定】
称取纯碱样品10.8g加入适量水,再加入过量CaCl2溶液,搅拌、过滤、洗涤、干燥后称得固体质量为10.0g,
请通过计算并结合右表判断此纯碱样品等级为 品.
【计算过程】
【总结反思】
某同学认为,在上述纯碱含量测定中,将CaCl2溶液改为BaCl2溶液,测定误差会减小,其理由是 .
【产品与原理】
该厂采用“侯氏制碱法”生产化工产品--纯碱(Na2CO3)和化肥NH4Cl.
生产原理是:将NH3和CO2通入饱和食盐水中得到NaHCO3和NH4Cl的混合物,反应为:
NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl;分离出NaHCO3,加热制得纯碱.
【生产流程】

【相关资料】
(1)NH4Cl
| ||
(2)已知20℃时有关物质的溶解度如下
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
【问题讨论】:
(1)操作Ⅰ、Ⅱ、Ⅲ中,相同操作的名称为
(2)反应①中发生了两个反应,写出其中的一个化学方程式:
(3)反应③中得到纯碱的化学方程式为:
(4)溶液B中的溶质有
(5)上述生产流程中可循环使用的是
A.挥发性气体C; B.溶液D; C.氢氧化镁;D.化肥NH4Cl
【组成确定】
(1)称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.
由上述实验可确定纯碱样品含有杂质
【含量测定】
称取纯碱样品10.8g加入适量水,再加入过量CaCl2溶液,搅拌、过滤、洗涤、干燥后称得固体质量为10.0g,
请通过计算并结合右表判断此纯碱样品等级为
【计算过程】
| 工业纯碱标准:(Na2CO3≥) | ||
| 优等品 | 一等品 | 合格品 |
| 99.2 | 98.8 | 98.0 |
某同学认为,在上述纯碱含量测定中,将CaCl2溶液改为BaCl2溶液,测定误差会减小,其理由是



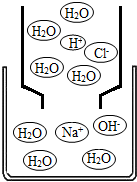 (2013?平江区二模)请写出下列相关的化学反应方程式并完成题后填空:
(2013?平江区二模)请写出下列相关的化学反应方程式并完成题后填空: