题目内容
【题目】下列图象能正确反映其对应关系的是( )
A. 恒温下,向一定质量的KNO3不饱和溶液中加入KNO3固体
恒温下,向一定质量的KNO3不饱和溶液中加入KNO3固体
B.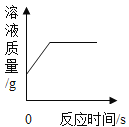 向一定量硝酸银溶液中加入一定量铜粉
向一定量硝酸银溶液中加入一定量铜粉
C.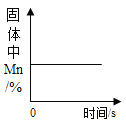 加热氯酸钾和二氧化锰的混合物
加热氯酸钾和二氧化锰的混合物
D.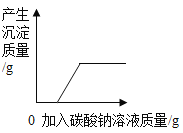 向含有盐酸和CaCl2的混合溶液中逐渐滴加Na2CO3溶液
向含有盐酸和CaCl2的混合溶液中逐渐滴加Na2CO3溶液
【答案】D
【解析】
A、恒温下,向一定质量的KNO3不饱和溶液中加入KNO3固体,硝酸钾逐渐溶解,溶质质量增加,溶质质量分数不断增加,待溶液达到饱和后,溶质质量分数不再变化,但是溶质质量分数不是从零开始变化,不符合题意;
B、向一定量硝酸银溶液中加入一定量铜粉,铜与硝酸银反应生成硝酸铜和银,![]() ,64份的铜置换出216份银,固体质量增加,溶液质量减小,待完全反应后,不再变化,不符合题意;
,64份的铜置换出216份银,固体质量增加,溶液质量减小,待完全反应后,不再变化,不符合题意;
C、加热氯酸钾和二氧化锰的混合物,氯酸钾分解为氯化钾和氧气,有气体生成,固体质量逐渐减小,锰元素质量不变,锰元素的质量分数逐渐增大,待氯酸钾完全反应后,不再变化,不符合题意;
D、向含有盐酸和CaCl2的混合溶液中逐渐滴加Na2CO3溶液,碳酸钠先与盐酸反应生成氯化钠、二氧化碳和水,待盐酸完全反应后,氯化钙和碳酸钠反应生成碳酸钙和氯化钠,故一开始无沉淀产生,随着反应的进行,沉淀质量逐渐增加,待氯化钙完全反应后,不再变化,符合题意。
故选D。

练习册系列答案
相关题目