题目内容
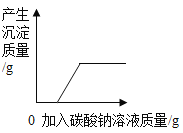
【题目】一定质量的碳酸钠和氯化钠固体混合物,加入101g水完全溶解后,再往其中加入100g氯化钙溶液,恰好完全反应.过滤,将滤渣干燥,称得其质量为10g,测得滤液中溶质的质量分数为10%。试计算:
(1)反应中所得滤渣为_____(填化学式);
(2)求所加氯化钙溶液溶质的质量分数________;
(3)求原固体混合物中碳酸钠的质量分数____________。
【答案】CaCO3 11.1% 53%
【解析】
(1)氯化钙能与碳酸钠反应生成碳酸钙沉淀和氯化钠,故反应中所得滤渣为碳酸钙,化学式为:CaCO3。
(2)解:由题意可知,过滤得到碳酸钙的质量是10g;
设所加氯化钙溶液溶质的质量分数为x,原固体混合物中碳酸钠的质量为y,反应生成的氯化钠的质量为z
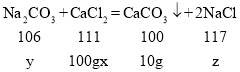
![]() x=11.1%
x=11.1%
![]() y=10.6g
y=10.6g
![]() z=11.7g
z=11.7g
答:所加氯化钙溶液溶质的质量分数为11.1%。
(3)测得滤液中溶质的质量分数为10%,设原固体混合物的质量为m,则:
![]() ,m=20g
,m=20g
原固体混合物中碳酸钠的质量分数为:![]()
答:原固体混合物中碳酸钠的质量分数为53%。

【题目】某兴趣小组利用废旧电话线中的金属铜丝进行了如下一系列实验。

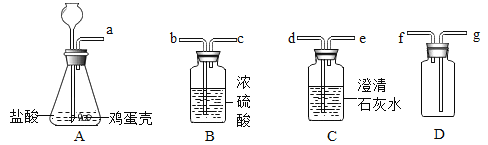
①如图所示,将铜丝分别放入盛有氯化锌溶液、稀硫酸、硝酸银溶液的试管中,观察到的现象是___________,发生反应的化学方程式为:___________。
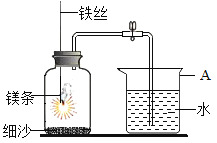
②用细线吊着的长玻璃棒的两端分别绕有40 cm长的铜丝(如图所示),使玻璃棒保持平衡,用酒精灯加热玻璃棒左端2分钟后冷却,可以观察到的现象是__________,产生该现象的原因是__________。
③为了研究金属铜生锈的条件,实验中将四段相同长度的铜丝分别按下图所示放置一个月,观察并记录现象如下:
E | F | G | H | |
实验装置 |
|
|
|
|
实验现象 | 铜丝不生锈 | 铜丝不生锈 | 铜丝不生锈 | 铜丝生锈 |
该实验设计体现的思想方法是_______________(选填:控制变量、对比与观察、定量分析、节能环保),结论:铜生锈是铜与 ______________作用的结果。