题目内容
【题目】以下是实验室常用的部分仪器。
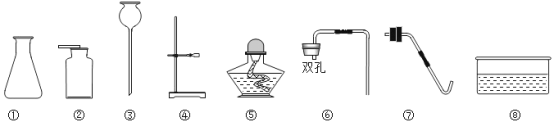
(1)仪器③的名称是________;
(2)用双氧水和二氧化锰混合物制氧气时,选用的发生装置是______(填仪器的序号,下同)
(3)同学们用浓盐酸和块状石灰石反应制取二氧化碳,并将得到的气体通入澄清石灰水中,始终没有发现澄清石灰水变浑浊。小英认为澄清石灰水已经变质:小青认为得到的CO2中混有_____(填名称)气体。他们为了证明自己的猜想进行了如下实验:
①小英将气体通入到新制的澄清石灰水中,但仍未发现澄清的石灰水变浑浊;
②小青取______与块状石灰石反应制取的CO2,并将产生的气体通入原澄清石灰水中,变浑浊,请写出石灰水变浑浊的化学方程式_________。
(4)乙炔是一种无色、无味、难溶水的气体。密度和空气接近,收集乙炔气体可选用的装置是_______。
【答案】长颈漏斗 ①③⑥ 氯化氢 稀盐酸 CO2+Ca(OH)2=CaCO3↓+H2O ②⑦⑧
【解析】
(1)长颈漏斗方便加液体药品;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,选用的发生装置是:①③⑥;
(3)浓盐酸有挥发性,挥发出的氯化氢气体能和氢氧化钙反应生成氯化钙和水,用浓盐酸和块状石灰石反应制取二氧化碳,并将得到的气体通入澄清石灰水中,始终没有发现澄清石灰水变浑浊,可能是得到的CO2中混有氯化氢气体。①小英将气体通入到新制的澄清石灰水中,但仍未发现澄清的石灰水变浑浊,说明不变浑浊的原因不是澄清石灰水变质;②小青取稀盐酸与块状石灰石反应制取的CO2,并将产生的气体通入原澄清石灰水中,变浑浊,因为二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;故答案为:氯化氢;②稀盐酸;CO2+Ca(OH)2=CaCO3↓+H2O;
(4)乙炔是一种无色、无味、难溶水的气体,密度和空气接近,因此最好用排水法收集;故答案为:②⑦⑧。

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案【题目】为了分析某生铁中铁的含量,学习小组的同学们进行了实验探究,即取6g生铁与10%的盐酸反应,加入盐酸质量与放出气体质量的关系如下表。(说明:生铁中杂质不溶于水,也不与盐酸反应)
盐酸质量/g | 36.5 | 73 | 109.5 | 146 |
气体质量/g | 0.1 | 0.2 | 0.2 | m |
(1)上述表格中m的值为 ;
(2)该生铁中铁的质量分数为多少?(写出计算过程,最终结果保留到0.1%)