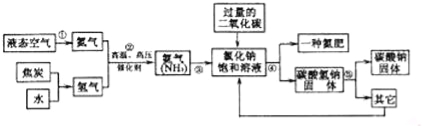
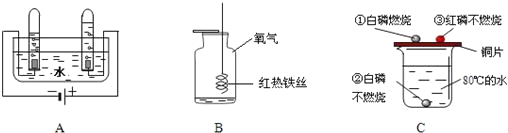
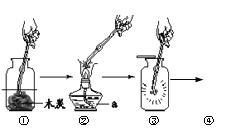
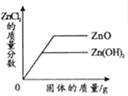��Ŀ����
����Ŀ��ijʯ��ʯ��Ʒ�е����ʼȲ�����ˮҲ�������ᷴӦ���ֳ�ȡ40gʯ��ʯ��Ʒ���ȷ�Ϊ4�ݣ��ֱ���Ϊ�٢ڢۢܣ���ÿ����Ʒ�ֱ���һ������ϡ���ᷴӦ���������������ʾ��
��Ʒ��� | �� | �� | �� | �� |
ϡ���������/g | 25 | 50 | m | 150 |
ʣ����������/g | 7.5 | 5 | 2 | 2 |
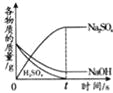
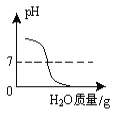
����Ţ�������Һ���ˣ�ȡ��Һ������![]() ���ձ��У������в��ϵμ���������Ϊ10.6%��̼������Һֱ���������ٲ���Ϊֹ���йس��������ı仯��ͼ��ʾ����ش��������⣺
���ձ��У������в��ϵμ���������Ϊ10.6%��̼������Һֱ���������ٲ���Ϊֹ���йس��������ı仯��ͼ��ʾ����ش��������⣺

��1����ʯ��ʯ��Ʒ�Ĵ���Ϊ_____��������Һ��������������Ϊ_____��
��2����Ţ����õ�ϡ���������mΪ����_____��
��3��A�㴦��Ӧ����Һ��������_____���û�ѧʽ��ʾ����
���𰸡�80%�� 7.3%�� 100g�� NaCl��
��������
����ǰ����ʵ���֪ÿ25g������ٹ���2.5g����ÿ25gϡ������2.5g̼���ǡ����ȫ��Ӧ���������Ĵι��廹ʣ2g��˵���������Ѿ���ȫ��Ӧ����ʣ��2g���ʡ���ʯ��ʯ��Ʒ�Ĵ���Ϊ![]() ��
��
��������Һ��������������Ϊ x
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 73
2.5g 25gx
![]()
x��7.3%
����ȡ��Һ������![]() ���ձ��У������в��ϵμ���������Ϊ10.6%��̼������Һֱ���������ٲ���Ϊֹ������̼������Һ������Ϊ25g����ȡ��Һ������
���ձ��У������в��ϵμ���������Ϊ10.6%��̼������Һֱ���������ٲ���Ϊֹ������̼������Һ������Ϊ25g����ȡ��Һ������![]() ����Ӧ���������Ϊy��
����Ӧ���������Ϊy��
������Ԫ�غ���Ԫ���غ�ɵù�ϵʽΪ
2HCl������������2NaCl��������Na2CO3
73 106
7.3%y 10.6%��25g
![]()
y��25g��
��Ţ����õ�ϡ���������mΪ25g��4��100g
��A�㴦��Ӧ����Һ���������ɵ��Ȼ��ƣ���Ӧ�Ļ�ѧʽΪNaCl��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ������У��й����ı仯ͼ�������Ӧ����������ǣ� ��
A | B | C | D |
|
|
|
|
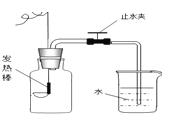
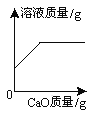
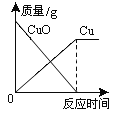
��ӽ����͵�NaCl��Һ�м������NaCl | �������������������������ϡ�����зֱ����������ZnO��Zn��OH��2 | ��Na2CO3��Һ�м���һ����������������NaOH��Һ | ��������������������H2SO4��Һ��NaOH��Һ��� |
A��A B��B C��C D��D