题目内容
【题目】A、B、C、D、E、F、G是初中化学常见的七种物质,化学兴趣小组同学设计了如图所示的接龙游戏,箭头表示一种物质可以转化成另一种物质。若常温下A是一种无色液体,B、C为无色无味气体:A转化成E为放热反应,且E、F物质类别相同,D、G物质类别相同,E与G反应可生成F。
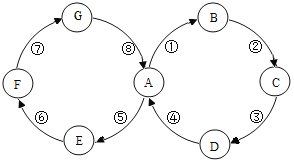
(1)A的一种实验室用途是______;B物质的化学式为______。
(2)转化⑥的化学方程式为______。
(3)下列有关说法中,错误的是______(填字母)。
A F固体溶于水时会出现放热现象
B 转化①、③、⑤分别对应的反应类型为分解反应、复分解反应、化合反应
C 转化②一定是化合反应
D C和F可反应,反应现象为有白色沉淀产生
【答案】做溶剂配制溶液等 O2 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH BCD
【解析】
(1)若常温下A是一种无色液体,那么A是水,水常用做溶剂配制溶液等;B、C为无色无味气体,水在通电的条件下生成氢气和氧气,碳和氧气在点燃的条件下生成二氧化碳,因此B是氧气,C是二氧化碳;故答案为:做溶剂配制溶液等;O2;
(2)氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,配平即可;故答案为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)A.F是氢氧化钠,氢氧化钠固体溶于水时会出现放热现象正确;B.转化①、③、⑤分别对应的反应类型为分解反应、复分解反应、化合反应错误,因为③不是复分解反应;C.转化②一定是化合反应错误,如甲烷和氧气在点燃的条件下生成二氧化碳和水;D.C和F可反应,反应现象为有白色沉淀产生错误,因为二氧化碳与氢氧化钠反应无现象;故答案为:BCD;
本题属于推断题,根据题目给出的流程图和信息:若常温下A是一种无色液体,那么A是水,水常用做溶剂配制溶液等;B、C为无色无味气体,水在通电的条件下生成氢气和氧气,碳和氧气在点燃的条件下生成二氧化碳,因此B是氧气,C是二氧化碳;A转化成E为放热反应,氧化钙和水反应生成氢氧化钙,因此E是氢氧化钙;且E、F物质类别相同,D、G物质类别相同,E与G反应可生成F,氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,因此F是氢氧化钠,G是碳酸钠,D也是碳酸盐。

【题目】实验室常用过氧化氢溶液和二氧化锰(催化剂)制取氧气。
【提出问题】催化剂二氧化锰的用量对反应速率是否有影响?
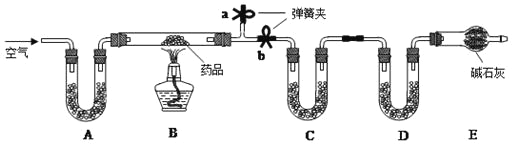
【设计实验】(1)实验装置如图所示:


![]() (2)实验记录:实验数据如下表:
(2)实验记录:实验数据如下表:
过氧化氢体积(ml) | 过氧化氢浓度 | 二氧化锰质量(g) | 测量数据(ml) | |
Ⅰ | 30 | 5% | 0.1 | |
Ⅱ | 30 | 5% | 0.2 | |
Ⅲ | 30 | 5% | 0.3 |
【实验分析】(1)过氧化氢分解的文字表达式为____________________;二氧化锰可作为该反应的催化剂的依据是__________________。
(2)表格中的“测量数据”是:相同时间内_______________________
(3)本实验中,测定待测数据的装置(上图中虚线框里)是_______(填编号)。
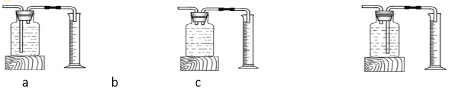
(4)若第Ⅱ次比第Ⅲ次实验的“测量数据”更______(填“大”或“小”)说明催化剂的用量越多,反应更快。
【实验反思】除了上述因素会影响过氧化氢的反应速率外,_________(写一种)也会影响过氧化氢的分解反应速率,请写出你的实验方案:_______________________
【题目】某石灰石样品中的杂质既不溶于水也不与盐酸反应。现称取40g石灰石样品,等分为4份(分别编号为①②③④),每份样品分别与一定量的稀盐酸反应,所得数据如表所示:
样品编号 | ① | ② | ③ | ④ |
稀盐酸的质量/g | 25 | 50 | m | 150 |
剩余固体的质量/g | 7.5 | 5 | 2 | 2 |
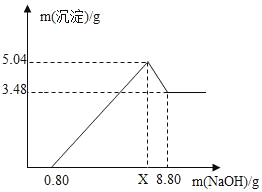
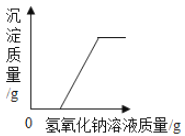
将编号③所得溶液过滤,取滤液质量的![]() 于烧杯中,向其中不断滴加质量分数为10.6%的碳酸钠溶液直至沉淀不再产生为止,有关沉淀质量的变化如图所示,请回答下列问题:
于烧杯中,向其中不断滴加质量分数为10.6%的碳酸钠溶液直至沉淀不再产生为止,有关沉淀质量的变化如图所示,请回答下列问题:
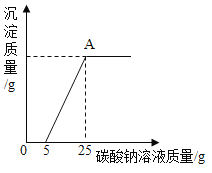
(1)该石灰石样品的纯度为_____;盐酸溶液的溶质质量分数为_____。
(2)编号③所用的稀盐酸的质量m为多少_____?
(3)A点处对应的溶液中溶质是_____(用化学式表示)。