题目内容
【题目】托盘天平是化学实验室中的常用仪器,如图是托盘天平的示意图,请你回答下列问题:
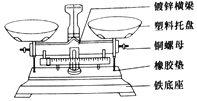
(1)制作托盘天平的材料中属于有机合成材料的是______,属于金属材料的是______(均填一种).
(2)写出一种防止托盘天平底座锈蚀的方法:______;
(3)金属铁在生产、生活中应用广泛,炼铁的原理是一氧化碳与氧化铁的反应,写出该反应的化学方程式:______;其中一氧化碳表现______性.
【答案】塑料(或橡胶) 铜(或锌或铁) 保持天平底座洁净干燥 Fe2O3+3CO![]() 2Fe+3CO2 还原
2Fe+3CO2 还原
【解析】
(1)塑料、橡胶属于有机合成材料,铜、锌、铁属于金属材料。制作托盘天平的材料中属于有机合成材料的是塑料(或橡胶),属于金属材料的是铜(或锌或铁;
(2)为了防止金属的锈蚀,人们常采用在其表面刷油漆、涂油或镀上其他金属等覆盖保护膜的方法,还可以保持天平底座洁净干燥;
(3)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO![]() 2Fe+3CO2。
2Fe+3CO2。

【题目】鸡蛋壳的主要成分是碳酸钙。为了测定某鸡蛋壳中碳酸钙的质量分数,小军同学进行了如下实验:
将鸡蛋壳洗净、干燥并捣碎后,与足量稀盐酸在烧杯中反应(假设鸡蛋壳中杂质不与稀盐酸反应)。
有关实验数据如表:
反应前 | 反应后 | ||
实验 数据 | 稀盐酸的质量 | 鸡蛋壳的质量 | 剩余物的质量 |
100g | 12g | 108.7g | |
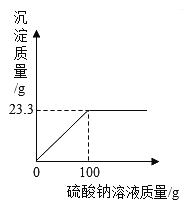
(1)根据质量守恒定律可知,反应中产生二氧化碳气体______g。
(2)计算该鸡蛋壳中碳酸钙的质量_____。
【题目】老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种。同学们对该粉末进行了定性与定量研究。
(1)定性实验:
实验方案 | 实验现象 | 实验结论 |
取少量红色粉末放入试管 中,滴加足量的稀盐酸振荡 | 红色粉末全部消失,溶液呈棕黄色 | 粉末为Fe2O3 |
_____ | 粉末Cu |
写出“红色粉末全部消失”发生反应的化学方程式_____。
(2)定量实验:
取该粉末4g放入硬质玻璃管中,先通CO,然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却。实验装置如图:
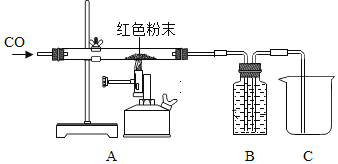
①实验时,先通CO再加热的目的是_____。
②若该粉末全部是氧化铁,在硬质玻璃管中观察到的实验现象是_____。B装置是用于吸收二氧化碳并收集CO,其中盛放的试剂最好是_____。
A NaOH溶液 B 稀盐酸 C 水
如果该实验没有装置B、C,实验造成的危害是_____。
③若该粉末为铜粉和氧化铁的混合物,待装置完全冷却至室温,称量硬质玻璃管内剩余固体的质量为mg。则m的取值范围是_____。