题目内容
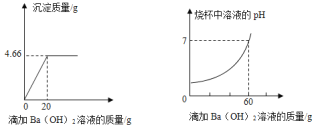
【题目】某混合溶液中含有硫酸和盐酸,取该混合溶液20g于烧杯中,不断滴加氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH的变化如图所示(BaCl2溶液呈中性)。求:
(1)完全反应后生成沉淀的质量为_____g;
(2)与盐酸反应的氢氧化钡溶液质量为_______g;
(3)原混合溶液中硫酸的质量分数是多少_____?
【答案】4.66g 40 9.8%
【解析】
(1)由图可知,反应后生成硫酸钡沉淀的质量为4.66g,故填4.66;
(2)由图可知,与盐酸和硫酸恰好完全反应后消耗的氢氧化钡溶液的质量为60g,其中与硫酸反应的氢氧化钡溶液的质量为20g,所以与盐酸反应的氢氧化钡溶液质量为60g20g=40g,故填40;
(3)解:设参加反应的纯硫酸的质量为x
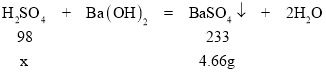
98:233=x:4.66g
x=1.96g
混合溶液中硫酸的质量分数是![]() ×100%=9.8%
×100%=9.8%
答:混合溶液中硫酸的质量分数是9.8%。

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目