题目内容
【题目】有一包粉末,已知由CaCO3、FeCl3、MgCl2、Na2SO4、NaOH、NaNO3中的几种组成.为确定其组成,现进行以下实验,各步骤均已充分反应.
①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
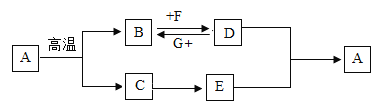
③将①步得到的无色溶液A进行如图所示的实验.

请回答下列问题:
(1)B的化学式是___.过滤操作中玻璃棒的作用是___.
(2)A中一定存在的溶质的化学式是___、___.
(3)向沉淀中加入稀盐酸,得到黄色溶液的化学方程式是___.
(4)生成白色沉淀D的化学方程式是___.
(5)这包粉末中可能含有物质的化学式是___、___.
【答案】BaSO4 引流 Na2SO4 NaCl 2Fe(OH)3+6HCl═2FeCl3+3H2O NaCl+AgNO3═AgCl↓+NaNO3 MgCl2 NaNO3
【解析】
(1)由题干可知,粉末中的硫酸钠能和硝酸钡反应生成硝酸钠和硫酸钡沉淀,所以白色沉淀B是硫酸钡,其化学式是BaSO4,故填BaSO4;
过滤操作中玻璃棒的作用是引流,故填引流。
(2)向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液,说明沉淀中含有碳酸钙和氢氧化铁,进而说明原物质中含有的碳酸钙、氯化铁,A溶液为无色液体,说明氯化铁全部与氢氧化钠反应生成了氯化钠和氢氧化铁沉淀,所以溶液A中一定含有氯化钠,步骤③中向A溶液中加入硝酸钡溶液生成白色沉淀,说明A溶液中,含有硫酸钠,若原物质中含有氯化镁也已形成氢氧化镁沉淀,而硝酸钠不影响本题的现象,所以A溶液中一定存在的溶质是硫酸钠和氯化钠,其化学式分别是Na2SO4、NaCl,故填Na2SO4、NaCl。
(3)向沉淀中加入稀盐酸,得到黄色溶液的反应是氢氧化铁与盐酸反应生成氯化铁和水,故反应的化学方程式写为:2Fe(OH)3+6HCl═2FeCl3+3H2O。
(4)生成白色沉淀D的反应是氯化钠和硝酸银反应生成硝酸钠和氯化银沉淀,故反应的化学方程式写为:NaCl+AgNO3═AgCl↓+NaNO3。
(5)通过上述实验不能确定粉末中是否含有MgCl2和NaNO3,所以这包粉末中可能含有物质的化学式氯化镁与硝酸钠,其化学式分别是MgCl2、NaNO3,故填MgCl2、NaNO3。

【题目】“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体。某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示。同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究。

(提出问题):久置固体的成分是什么?
(收集资料):
(1)、查阅资料:铁与氯化铁溶液在常温下生成氯化亚铁:Fe+2FeCl3═3FeCl2
(2)、打开固体包装观察:部分粉末呈黑色、部分粉末呈白色、另有少数红棕色的块状固体。
(作出猜想):久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3。
(实验探究):如表是甲组同学涉及并记录的实验报告,请你补充完整。
实验操作 | 实验现象 | 实验结论 |
一、取少量固体加入足量蒸馏水,搅拌溶解 | 固体部分溶解,并放出大量热 | 固体中一定含有_____。 |
二、过滤,取滤液滴加无色酚酞试液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
三、取滤渣加入足量稀盐酸 | 固体逐渐消失,产生大量无色气体,得到浅绿色溶液 | 固体中一定含有_____,一定不含有Fe2O3 |
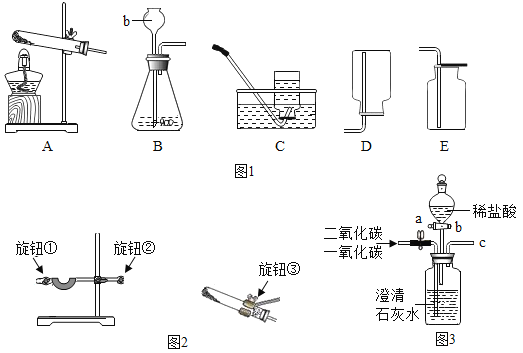
四、将操作三中产生的气体通入到澄清石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有_____。 |
(实验质疑):乙组同学认为甲组同学在实验中得出“一定不含有Fe2O3”的结论是错误的,理由是_____;你认为甲组同学哪一步操作得出的结论也不合理_____,理由是(用化学方程式表示)_____。
(继续探究):为验证固体中是否含有Fe2O3,乙组同学用磁铁先分离出铁粉,向残留固体中加入足量_____,若溶液呈棕黄色,证明固体中含有Fe2O3.写出溶液呈棕黄色的化学反应方程式_____。
【题目】某化学小组在实验室用CO和Fe2O3在密闭容器中隔绝空气加强热模拟炼铁过程,一段时间后收集到如下数据:
物质 | CO | Fe2O3 | Fe | M | CO2 |
反应前质量(g) | 2.8 | 16 | 0 | 0 | 0 |
反应后质量(g) | 0 | 0 | 0 | a | b |
(1)预期看到的实验现象应该是_____________________________;
(2)表中b的值为____________;物质M的化学式为_______________。