题目内容
【题目】(11分)现有10%的Na2CO3溶液,请按下面要求计算:
(1)106 g上述溶液中所含溶质量为 g;
(2)106 g 上述溶液与足量10%的盐酸反应,最多可生成CO2多少克?
(3)向106 g 上述溶液中逐滴加入10%的盐酸并不断搅拌,此时发生的反应为:
Na2CO3 + HCl =NaHCO3 + NaCl
当Na2CO3 全部转化为NaHCO3后,再加入盐酸才开始放出CO2 。请在“题25图”中画出产生气体的曲线。
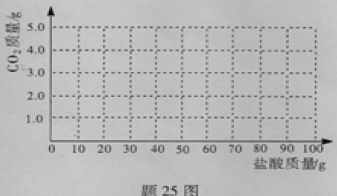
(4)另取10% Na2CO3溶液边搅拌边加入10%的盐酸,有关反应物与生成物的量如下表:
物质 | Na2CO3 | HCl | X | NaCl | CO2 | H2O |
质量/g | 31.8 | 14.6 | 16.8 | 23.4 | 4.4 | m |
则m= ;该反应的化学方程式为 。
【答案】(1)10.6 g;(2)4.4g
(3)
(4)1.8 3Na2CO3+ 4HCl===2NaHCO3+4NaCl+ H2O + CO2↑
【解析】
试题分析:(1)该溶液溶质质量为106×10%=10.6g;(2)由碳酸钠质量10.6g,再据碳酸钠与盐酸反应生成氯化钠、水和二氧化碳化学反应方程式可计算出生成二氧化碳质量为4.4g;
解:设最多生成二氧化碳的质量为x,则:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
106 44
10.6g x
106 / 10.6g =44/x x=4.4g
(3)由碳酸钠质量为10.6g再据 Na2CO3+ HCl===NaHCO3+NaCl 可计算出消耗的氯化氢为3.6g即盐酸的质量为3.65g÷10%=36.5g,则从消耗盐酸36.5g起,开始有二氧化碳产生,该反应生成了8.4g碳酸氢钠,再据碳酸氢钠与盐酸反应生成氯化钠,水,二氧化碳可知,再消耗36.5g盐酸则碳酸氢钠完全反应即总共消耗36.5g+36.5g=73g盐酸的时候完成反应生成4.4g二氧化碳。
(4)由质量守恒定律可知,反应前后物质的质量总和不变,所以可计算出水的质量为1.8g;
31.8gNa2CO3中钠元素的质量为 13.8g,23.4gNaCl中钠元素是9.2g,由元素守恒可知X为碳酸氢钠,
写出各反应物、生成物,配平,可得方程式:3Na2CO3+ 4HCl===2NaHCO3+4NaCl+ H2O + CO2↑

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
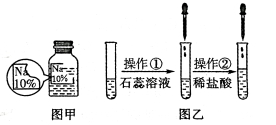
期末金牌卷系列答案【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。