题目内容
【题目】将 20g由NaCl和CaCl2组成的固体混合物,溶于水配成50g溶液, 向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,加入Na2CO3溶液的质量与所得沉淀的质量关系如下表:
Na2CO3溶液的质量/g | 2 0 | 4 0 | 6 0 | 8 0 | 1 0 0 |
生成沉淀的质量/g | 4 | 8 | x | 10 | 10 |
(1)x的值为 。
(2)求所加Na2CO3 溶液中溶质的质量分数(写出计算过程)。
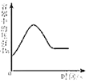
(3)画出产生沉淀与所加Na2CO3溶液质量关系的曲线图。
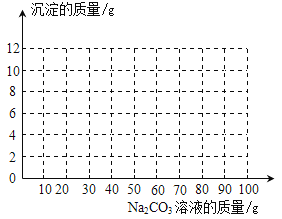
【答案】(1)10;(2)21.2%;(3) 
【解析】
(1)由表分析可得加入20g碳酸钠沉淀质量增加4g,加入80g碳酸钠溶液最终只生成10g沉淀说明氯化钙不足,只能生成10g沉淀,故填:10g。
(2)根据实验数据,加入20g碳酸钠溶液完全反应可生成沉淀质量为4g,
解:设生成4g沉淀需Na2CO3质量为x

碳酸钠的质量分数是: ![]() ×100%=21.2%
×100%=21.2%
答:原混合物中碳酸钠的质量分数是21.2%。
(3)由分析可得20g碳酸钠生成4g碳酸钙,故生成10g碳酸钙沉淀需要50g碳酸钠溶液,用图表示 。
。

练习册系列答案
相关题目