题目内容
取只含碳酸氢钙的硬水a g,充分加热,发生如下反应:
Ca(HCO3)2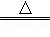 CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
(1)碳酸氢钙中钙元素与氧元素的质量比为 。
(2)计算此硬水中碳酸氢钙的质量是多少?
(3)将a g这样的硬水充分煮沸,理论上可得到的软水质量为 。
Ca(HCO3)2
 CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:(1)碳酸氢钙中钙元素与氧元素的质量比为 。
(2)计算此硬水中碳酸氢钙的质量是多少?
(3)将a g这样的硬水充分煮沸,理论上可得到的软水质量为 。
(1)5:12;(2)1.62g;(3)(a﹣1.44)g.
(1)碳酸氢钙中钙元素和氧元素的质量比为:40:(16×6)=5:12;
(2)设Ca(HCO3)2的质量为x,生成二氧化碳的质量为y
Ca(HCO3)2 CaCO3↓+CO2↑+H2O
CaCO3↓+CO2↑+H2O
162 100 44
x 1.0 g y
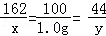
解得:x=1.62g,y=0.44g;
答:硬水中碳酸氢钙的质量是1.62g;
(3)将ag这样的硬水充分煮沸,理论上可得到的软水质量为:(a﹣1.0g﹣0.44g)=(a﹣1.44)g.
(2)设Ca(HCO3)2的质量为x,生成二氧化碳的质量为y
Ca(HCO3)2
 CaCO3↓+CO2↑+H2O
CaCO3↓+CO2↑+H2O162 100 44
x 1.0 g y
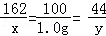
解得:x=1.62g,y=0.44g;
答:硬水中碳酸氢钙的质量是1.62g;
(3)将ag这样的硬水充分煮沸,理论上可得到的软水质量为:(a﹣1.0g﹣0.44g)=(a﹣1.44)g.

练习册系列答案
相关题目