题目内容
下图是实验室所用盐酸试剂瓶上标签的部分内容,、请仔细阅读后计算:

(1)欲配制100g溶质质量分数为14.6%的稀盐酸,需用这种盐酸多少毫升? (计算结果精确到0.1)
(2)取上述配制得到的稀盐酸50g与足量锌充分反应后,理论上可制得氢气多少克?反应后所得溶液的溶质质量分数是多少?(计算结果精确到0.1)

(1)欲配制100g溶质质量分数为14.6%的稀盐酸,需用这种盐酸多少毫升? (计算结果精确到0.1)
(2)取上述配制得到的稀盐酸50g与足量锌充分反应后,理论上可制得氢气多少克?反应后所得溶液的溶质质量分数是多少?(计算结果精确到0.1)
(1)33.8ml
(2)0.2g 24.2%
(2)0.2g 24.2%
(1)设需用盐酸的体积为x
100g×14.6%=x×1.20g/cm3×36%
解得x=33.8mL.
(2)设生成的氢气的质量为y,生成氯化锌的质量为z,参加反应的锌质量为m
Zn+2HCl=ZnCl2 +H2↑
65 73 136 2
m 50g×14.6% z y
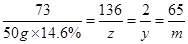
解得y=0.2g.z=13.6g,m=6.5g
溶液的质量为:50g+6.5g-0.2g=56.3g
故溶质的质量分数为: ×100%=24.2%
×100%=24.2%
100g×14.6%=x×1.20g/cm3×36%
解得x=33.8mL.
(2)设生成的氢气的质量为y,生成氯化锌的质量为z,参加反应的锌质量为m
Zn+2HCl=ZnCl2 +H2↑
65 73 136 2
m 50g×14.6% z y
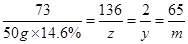
解得y=0.2g.z=13.6g,m=6.5g
溶液的质量为:50g+6.5g-0.2g=56.3g
故溶质的质量分数为:
 ×100%=24.2%
×100%=24.2%
练习册系列答案
相关题目
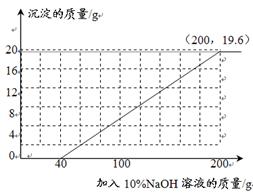
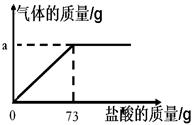

 CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题: