题目内容
【题目】某面包膨松剂由碳酸氢钠和碳酸氢铵两种物质组成。它在面包制作过程中发生分解反应。化学小组为验证该膨松剂的成分,查阅资料,设计如图所示实验(实验开始前弹簧夹都处于关闭状态)。
资料:①碳酸氢铵加热分解成三种气体(含水蒸气);
②通常状况下,1体积水溶解700体积氨气,氨气溶于水所得溶液为氨水。
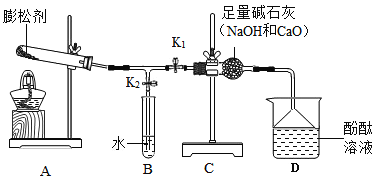
(1)A装置中,膨松剂在加热过程中发生两个分解反应:![]() ;关闭K1,打开K2,充分加热当看见______现象时,说明有碳酸氢铵存在。打开K2,关闭K1,当看见______现象时,说明有碳酸氢钠存在。是否需要将装置B中的水换成澄清石灰水,说明理由。________
;关闭K1,打开K2,充分加热当看见______现象时,说明有碳酸氢铵存在。打开K2,关闭K1,当看见______现象时,说明有碳酸氢钠存在。是否需要将装置B中的水换成澄清石灰水,说明理由。________
(2)如果没有装置C,可能会对实验造成的影响是什么?______
【答案】酚酞溶液变红 A中试管底部仍有固体残留物 不需要,装置B中水的作用只是判断试管内反应是否进行完全(没有气泡说明反应完了) 不能检验出碳酸氢铵的存在
【解析】
(1)加热碳酸氢铵分解生成氨气、水和二氧化碳,氨气溶于水显碱性,可使酚酞变红;碳酸氢钠分解生成碳酸钠固体和水、二氧化碳,所以打开K1,关闭K2,充分加热当看见酚酞溶液变红现象时,说明有碳酸氢铵存在;打开K2,关闭K1,当看见A中试管底部仍有固体残留物现象时,说明有碳酸氢钠存在;
不需要将装置B中的水换成澄清石灰水,装置B中水的作用只是判断试管内反应是否进行完全(没有气泡说明反应完了)。当B中水里没有气泡,试管中有剩余固体存在时,因为碳酸氢铵分解后无固体,所以可以说明有碳酸氢钠存在,而通过氨气的检验可以证明碳酸氢铵的存在,进而可以证明该面包膨松剂由碳酸氢钠和碳酸氢铵两种物质组成。因此,不需要将装置B中的水换成澄清石灰水。
(2)二氧化碳溶于水形成碳酸,可以和氨水发生反应,如果不除去二氧化碳,会影响对氨气的判断,进一步会影响对碳酸氢铵的判断,所以如果没有装置C,可能会对实验造成的影响是:不能检验出碳酸氢铵的存在。

【题目】(1)用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液pH变化曲线如图所示:

①该反应的化学方程式是________________;
②该实验操作是将__________(写溶质的化学式)溶液逐滴加入到另一种溶液中。
(2)若用稀硫酸代替(1)中的稀盐酸,将稀硫酸逐滴加入至盛有氢氧化钠溶液的烧杯中,当滴加到一定量并充分反应时,请对烧杯中溶质成分进行探究。
(提出问题)此时烧杯中的溶质成分是什么?
(猜想与假设)Ⅰ:Na2SO4;Ⅱ:_____________;Ⅲ:Na2SO4和NaOH。
(实验与探究)
实验步骤 | 实验现象 | 实验结论 |
取少量上述烧杯中的溶液于试管中,滴加_______溶液 | _______________ | 猜想Ⅱ正确 |
取少量上述烧杯中的溶液于试管中,滴加_______溶液 | ______________ | 猜想Ⅲ正确 |