题目内容
向20g赤铁矿样品中(样品中杂质不溶于水,也不和酸反应)不断加入稀盐酸至固体量不再减少为止,共消耗稀盐酸184g,测得剩余固体的质量为4g。请计算:
(1)赤铁矿样品中,氧化铁的质量分数
(2)最后所得溶液中溶质的质量分数
(1)80%; (2)16.25%
解析试题分析:已知量:20g赤铁矿样品,稀盐酸184g,剩余固体的质量为4g;未知量:氧化铁的质量,所得溶液中溶质的质量分数;思路分析:发生的反应为:Fe2 O3 + 6HCl="==2" FeCl3 + 3H2O;已知数据均为混合物的质量;由已知数据可以求得样品中氧化铁的质量,所得溶液的质量,再结合化学方程式即可求得所得溶质的质量,利用溶质质量分数的计算公式即可解答。
解: (1)样品中氧化铁的质量是20g — 4 g ="=" 16 g ……………………………… 1分
样品中,氧化铁的质量分数为  ×100% ="=" 80%…………………… 1分
×100% ="=" 80%…………………… 1分
(2)设:所得溶液中溶质质量为x,则
Fe2 O3 + 6HCl===2 FeCl3 + 3H2O ……………………………………… 1分
160 325
16g X 
X ="=" 32.5g …………………………………………………… 1分
所得溶液的质量为:184 g + 20 g — 4 g ="=" 200 g …………………………… 1分
所得溶液中溶质的质量分数为 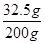 ×100% ==16.25% …………………………1分
×100% ==16.25% …………………………1分
答:(1)赤铁矿样品中,氧化铁的质量分数80% ;(2)最后所得溶液中溶质的质量分数16.25%
考点: 化学方程式计算;质量守恒定律

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目