题目内容
【题目】用化学用语的化学式或化学符号填空:
(1)两个氮分子:_____;
(2)地壳中含量最高的元素_____;
(3)氧化铁中铁元素显正三价:_____;
(4)3个铝离子_____;
(5)碳酸钠:_____;
(6)4个硅原子_____;
(7)保持水化学性质的微粒_____。
【答案】2N2 O ![]() 3Al3+ Na2CO3 4Si H2O
3Al3+ Na2CO3 4Si H2O
【解析】
(1)由化学式的表示方法,N2可表示一个氮分子,两个氮分子就是在氮气化学式的前面加上数字2,故填2N2;
(2)地壳中含量最高的元素是氧元素,故填O;
(3)氧化铁中铁元素显正三价,化合价的表示方法是在元素符号的正上方标出正负号和数字,正负号在前,数字在后,故填![]() ;
;
(4)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,3个铝离子就是在铝离子的前面加上数字3,故填3Al3+;
(5)碳酸钠中钠元素为+1价,碳酸根为﹣2价,根据化合物中各元素化合价的代数和为零,其化学式为Na2CO3,故填Na2CO3;
(6)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故4Si可表示4个硅原子,故填4Si;
(7)保持水的化学性质的微粒是水分子,H2O可表示水分子,故填H2O。

【题目】空气中氧气含量测定的再认识。
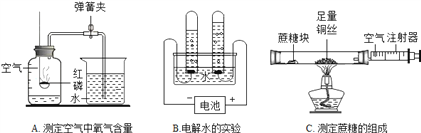
请回忆教材用红磷燃烧来粗略测定空气中氧气含量的装置。
(1)写出红磷燃烧的反应化学方程式_____,属_____反应(填“化合”或“分解”)。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内_____减小,烧杯中水倒吸到集气瓶。若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
(问题提出)有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大。
(实验改进)
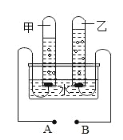
Ⅰ.根据铁在空气中生锈的原理设计下图实验装置,再次测定空气中氧气含量。装置中饱和食盐水、活性炭会加速铁生锈。

Ⅱ.测得实验数据如下表
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
(交流表达)
(1)铁生锈过程发生复杂的化学反应(一个缓慢氧化的过程),首先是铁与氧气、水反应生成氢氧化亚铁,写出氢氧化亚铁的符号_____。然后生成氢氧化铁。最终生成铁锈。
(2)根据表中的数据计算,改进实验后测得空气中氧气体积分数是_____(计算结果精确到0.1%)。
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:_____。