题目内容
【题目】维生素C(简称Vc,又名抗坏血酸)易溶于水,水溶液呈酸性,易被O2、I2(碘)氧化。某同学为了探究Vc的性质,进行了如下实验。
实验1:用某制药厂生产的Vc片(每片含Vc0.1g及不溶性辅料)配制0.5%的Vc溶液。
(1)若取5片Vc片,应大约取蒸馏水____mL(取整数)
(2)量取蒸馏水除了用到量筒外还需用到的仪器是_____。
实验2:设计实验证明 Vc 溶液具有酸性。
(3)限用试剂:无色酚酞溶液、稀氢氧化钠溶液。请你完成下表。
实验步骤 | 预期现象及结论 |
_______ | _______,说明Vc溶液具有酸性 |
实验3:探究Vc溶液在一定温度下(18℃)露置时间对Vc含量的影响,采用控制变量法进
行实验,具体如下表所示。 (信息提示:淀粉与碘作用显蓝色。往碘水中加入几滴淀粉溶液,然后逐滴加入Vc溶液,当溶液的蓝色褪去,说明碘与Vc恰好完全反应。)
实验 序号 | 碘水浓度 及用量 | 淀粉溶液 | Vc 溶液恒温露置时间/h | 蓝色消失需要 Vc 溶液滴数 |
① | 0.06%、4.8mL | 3 滴 | 0 | 10 |
② | 0.06%、4.8mL | 3 滴 | 12 | 12 |
③ | 3 滴 | 24 | 18 | |
④ | 0.06%、4.8mL | 3 滴 | 36 |
(4)实验③中碘水浓度及用量分别是_____。
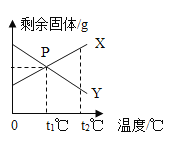
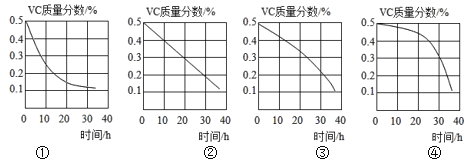
(5)Vc质量分数随露置时间(0~36h)的变化图像,正确的是____(填图像标号)。
(6)为了提高定量探究Vc溶液的准确性,配制Vc溶液时,必须先除去溶解在蒸馏水中的少量O2,具体处理方法是_____。
【答案】100ml 胶头滴管 向氢氧化钠溶液中加入酚酞,溶液变为红色,将Vc溶液逐滴滴入溶液中,并用玻璃棒不断的搅拌 红色消失 0.06%、4.8mL ③ 高温煮沸丙迅速冷却
【解析】
(1)5片Vc中含有Vc的质量为5×0.1g=0.5g,含Vc0.5g的0.5%的溶液的质量为0.5g÷0.5%=100g ,故需要加热水的质量为100g-0.5g=99.5g,故水的体积约为100ml。
(2)量取蒸馏水除了用到量筒外还需用到的仪器是胶头滴管。
(3)向氢氧化钠溶液中加入酚酞,溶液变为红色,将Vc溶液逐滴滴入溶液中,并用玻璃棒不断的搅拌,当观察到红色消失,说明Vc溶液显酸性。
(4)根据控制变量法,数据3中的数据要与其他数据相同,故填0.06%、4.8mL
(5)由表中的数据分析可知,随着时间的推移,Vc的质量分数逐渐降低,不成比例,且在相等的时间段内,时间越长,Vc溶液的质量分数降低的越快,故选③。
(6)升高温度可以降低气体的溶解度,故方法是高温煮沸。

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案