题目内容
【题目】下图是元素周期表中的一部分,请回答下列问题:
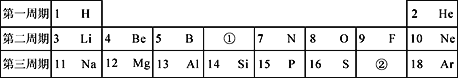
(1)上表中①所示元素的原子序数是______,②所示元素的单质的化学式是______。
(2)X3+与O2-的核外电子排布相同,则X的元素符号是_____,它处在元素周期表中第____周期,它与氧元素组成的化合物的名称是________。
(3)氟原子在化学反应中易____(填“得”或“失”)电子,所以氟元素在化合物中的化合价通常为______价。
【答案】6 Cl2 Al 三 氧化铝 得 -1
【解析】
(1)①是6号元素——碳,原子序数为6;②表示氯元素,氯元素组成的单质是氯气,其化学式为Cl2;
(2)O2-核外有10个电子,X3+与O2-的核外电子排布相同,则X是铝原子,其元素符号为Al;在元素周期表中位于第三周期;铝元素在化合物中显+3价,氧元素显-2价,二者组成的化合物是氧化铝;
(3)氟原子核外有9个电子,为达到稳定结构,故氟原子易得到1个电子,是最外层达到8个电子的稳定结构;氟原子得到一个电子后在化合物中该元素的化合价为-1价。

 阅读快车系列答案
阅读快车系列答案【题目】碘化钾(KI)是白色固体,保存不当会被氧化为单质碘(I2)而泛黄变质。实验小组为探究碘化钾变质原理,进行如下活动。
(查阅资料)
I.对于碘化钾变质的原理,有两种不同的反应:
甲:4KI+O2+2CO2==2K2CO3+2I2乙:4KI+O2+2X=4KOH+2I2
⑴请将上述方程式补充完整,X的化学式是_____。
Ⅱ.KOH与NaOH都属于碱,二者的化学性质相似。
(进行实验)实验1:探究变质的原理
取适量碘化钾固体暴露于空气一段时间,观察到固体泛黄。往泛黄的固体中加入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊。
⑵实验过程中产生的气体是_____。化学小组认为:据此现象,还不能得出“反应甲是造成碘化钾变质的原因”的结论。理由是_____。
(进行实验)实验2:探究变质的条件
分别取适量KI于燃烧匙中,再分别放入盛有不同物质的集气瓶中,塞紧胶塞,若干天后观察。
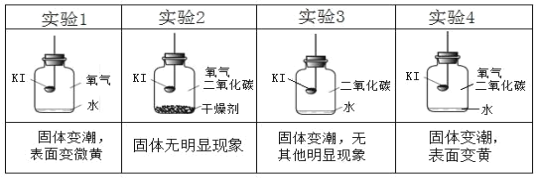
(解释与结论)
⑶对比实验_____(填序号),可以得出KI变质一定与水有关。对比实验_____(填序号),可以得出KI变质一定与氧气有关。
⑷从上述实验可推知,KI变质的条件是_____。
(提出问题)CO2的作用是什么?
(进行实验)
分别取10mL同浓度的KI溶液于3支试管中(试管编号1,2,3),再向试管2中通入CO2,向试管3中滴加几滴盐酸,分别用pH试纸测定溶液的pH;几分钟后,观察溶液的颜色。实验现象记录如下:
试管序号 | 1 | 2 | 3 |
溶液pH | pH=8 | pH=6 | pH=4 |
溶液颜色 | 无色 | 浅黄色 | 黄色 |
(解释与结论)
⑸①pH试纸的使用方法是_____。②CO2在KI变质过程中的作用是_____。
(反思与评价)
⑹探究KI变质条件时,同学们排除了氮气和稀有气体的影响,其原因是_____。
(拓展应用)
测定实验中使用的盐酸中所含溶质的质量分数。
⑺向烧杯中加入质量分数为10%的氢氧化钠溶液40g,再逐滴加入该盐酸,用pH计测定滴加过程中溶液的pH值。图2为滴加盐酸的质量与溶液pH的关系图。
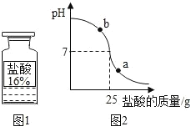
①a点对应的溶液中的溶质为_____(写化学式)。
②盐酸与氢氧化钠溶液反应是_____(选填“吸热”或“放热”)反应。
请以此次测定的数据,列式计算该盐酸的实际溶质质量分数。_____(写出计算过程)
⑻该盐酸的实际溶质质量分数与标签上标出的溶质质量分数不同的可能原因:_____(不考虑测量误差)。
【题目】维生素C(简称Vc,又名抗坏血酸)易溶于水,水溶液呈酸性,易被O2、I2(碘)氧化。某同学为了探究Vc的性质,进行了如下实验。
实验1:用某制药厂生产的Vc片(每片含Vc0.1g及不溶性辅料)配制0.5%的Vc溶液。
(1)若取5片Vc片,应大约取蒸馏水____mL(取整数)
(2)量取蒸馏水除了用到量筒外还需用到的仪器是_____。
实验2:设计实验证明 Vc 溶液具有酸性。
(3)限用试剂:无色酚酞溶液、稀氢氧化钠溶液。请你完成下表。
实验步骤 | 预期现象及结论 |
_______ | _______,说明Vc溶液具有酸性 |
实验3:探究Vc溶液在一定温度下(18℃)露置时间对Vc含量的影响,采用控制变量法进
行实验,具体如下表所示。 (信息提示:淀粉与碘作用显蓝色。往碘水中加入几滴淀粉溶液,然后逐滴加入Vc溶液,当溶液的蓝色褪去,说明碘与Vc恰好完全反应。)
实验 序号 | 碘水浓度 及用量 | 淀粉溶液 | Vc 溶液恒温露置时间/h | 蓝色消失需要 Vc 溶液滴数 |
① | 0.06%、4.8mL | 3 滴 | 0 | 10 |
② | 0.06%、4.8mL | 3 滴 | 12 | 12 |
③ | 3 滴 | 24 | 18 | |
④ | 0.06%、4.8mL | 3 滴 | 36 |
(4)实验③中碘水浓度及用量分别是_____。
(5)Vc质量分数随露置时间(0~36h)的变化图像,正确的是____(填图像标号)。
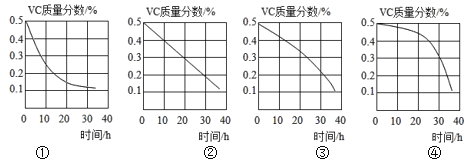
(6)为了提高定量探究Vc溶液的准确性,配制Vc溶液时,必须先除去溶解在蒸馏水中的少量O2,具体处理方法是_____。