题目内容
【题目】甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是
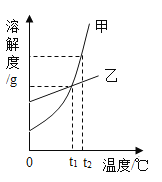
A.t2℃时,将甲、乙的两种饱和溶液分别降温到t1℃,所得溶液中溶质的质量分数相同
B.t1℃时,向50g水中加入甲可得80g饱和溶液,则乙在该温度下的溶解度为60g
C.“冬日捞碱,夏日晒盐”中的碱和盐可分别对应曲线中的甲和乙
D.t2℃时,将等质量的甲、乙两种溶液分别降温到0℃,甲溶液析出晶体质量多于乙
【答案】D
【解析】
A、t2℃时,将甲、乙的两种饱和溶液分别降温到t1℃,甲、乙物质的溶解度相等,所以所得溶液中溶质的质量分数相同,故A正确;
B、t1℃时,甲乙物质的溶解度相同,向50g水中加入甲可得80g饱和溶液,说明t1℃时甲的溶解度为60g,则乙在该温度下的溶解度为60g,故B正确;
C、甲物质的溶解度受温度变化影响较大,乙物质的溶解度受温度变化影响较小,所以“冬日捞碱,夏日晒盐”中的碱和盐可分别对应曲线中的甲和乙,故C正确;
D、t2℃时,甲、乙两种溶液是否饱和不能确定,所以分别降温到0℃,析出晶体质量也不能确定,故D错误。
故选:D。

练习册系列答案
相关题目
【题目】某小组用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁(如图所示)。下列表格中的各组物质或变化符合这种关系的是( )
选项 | 甲 | 乙 | 丙 | 丁 |
A | 化合物 | 盐酸 | MnO2 | 铁粉 |
B | 合成材料 | 合金 | 合成纤维 | 合成橡胶 |
C | 化学变化 | 置换反应 | 化合反应 | 复分解反应 |
D | 放热反应 | 硫在空气中燃烧 | NaOH溶液与稀H2SO4反应 | 高温分解石灰石 |
A.AB.BC.CD.D