题目内容
【题目】请结合如图实验装置回答有关问题:
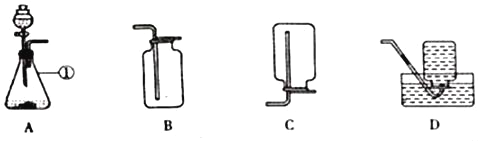
(1)写出装置A中标号①仪器的名称_____,若用A装置制取氧气,往该仪器里加入的固体药品是_____。
(2)写出实验室用过氧化氢溶液制取氧气的化学方程式_____。
(3)不能用装置C收集氧气的理由是_____;用装置D收集氧气,当观察到_____,说明已收集满。
【答案】锥形瓶 二氧化锰 2H2O2![]() 2H2O+O2↑ 氧气的密度大于空气密度 集气瓶口有大气泡出现时
2H2O+O2↑ 氧气的密度大于空气密度 集气瓶口有大气泡出现时
【解析】
(1)装置A中①仪器的名称是锥形瓶,实验室在此装置中利用过氧化氢和二氧化锰制取氧气,锥形瓶中放二氧化锰。分液漏斗中放过氧化氢溶液;
(2)过氧化氢溶液在二氧化锰的催化下生成水和氧气,方程式为:2H2O![]() 2H2O+O2↑;
2H2O+O2↑;
(3)因为氧气的密度大于空气密度可以使用向上排空气法收集,氧气不易溶于水,也可以用排水法收集,排水法收集氧气,当集气瓶口有大气泡出现时说明氧气已满;
故答案为:(1)锥形瓶;二氧化锰;(2)2H2O2![]() 2H2O+O2↑;(3)氧气的密度大于空气密度;集气瓶口有大气泡出现时;
2H2O+O2↑;(3)氧气的密度大于空气密度;集气瓶口有大气泡出现时;

【题目】(6分)我省两淮地区煤炭资源丰富,瓦斯存在于煤层及周围岩层中,是井下有害气体的总称,主要成分是甲烷。
(1)请你写出甲烷完全燃烧的化学方程式:__________________________________。
(2)煤矿瓦斯爆炸有两个必要条件:
①瓦斯含量在爆炸极限的范围内;②________________________________________。
(3)下表是常见三种气体的爆炸极限,请你据此判断:
最容易发生爆炸的气体是____。
可燃气体 | 爆炸极限(体积分数) |
H2 | 4.0%~74.2% |
CH4 | 5%~15% |
CO | 12.5%~74.2% |
(4)下列图标中,与燃烧和爆炸无关的是
![]()
A B C D
(5)某现代化的矿井采用了“低浓度瓦斯发电技术”,有效解决了矿区及周边地区的照明用电。这种既采煤又发电联合生产的优点是___________________________________。
【题目】下面是某实验小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务。
(研究课题)探究草酸晶体受热分解的产物。
(查阅资料)
(1)该小组同学通过网络查询,获得草酸及草酸晶体的一些相关知识:
名称 | 化学式 | 颜色、状态 | 溶解性 | 熔点(℃) | 密度(g/cm3) |
草酸 | H2C2O4 | ﹣ | 易溶于水 | 189.5 | 1.900 |
草酸晶体 | H2C2O42H2O | 无色晶体 | ﹣ | 101.5 | 1.650 |
(2)白色的无水硫酸铜遇水蒸气会变蓝色
(作出猜想)第一种:草酸分解产物CO2和H2第二种:草酸分解产物是CO2、CO 和H2O
第三种:草酸的分解产物是 CO2、CO 和 H2
(设计实验)
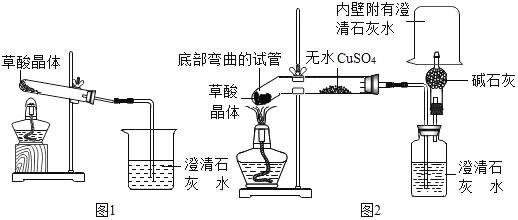
(实验操作)
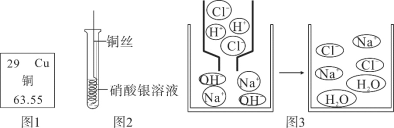
甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊,乙同学按图2的装置实验也观察到澄清的石灰水变浑浊,且无水 CuSO4变蓝。若产物中有 CO,则图二中玻璃尖嘴处用火柴点燃观察到的实验现象是_____。
(得出结论)若第二种猜想是正确的,请你写出草酸分解的反应方程式_____。
(反思评价)乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到 182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验。
①请你谈谈图二装置比较图一装置的优点(写出一点)_____。
②利用图二设计的装置证明产物中没有 H2的方法是:_____。