题目内容
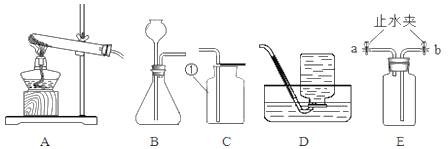
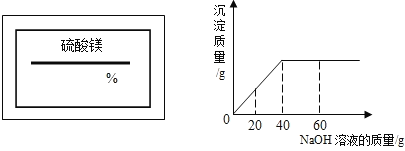
【题目】某同学在实验室发现一瓶标签残缺(如图所示)的溶液.为了测定此溶液的溶质质量分数,他取出![]() 该溶液,向其中逐滴加入溶质质量分数为
该溶液,向其中逐滴加入溶质质量分数为![]() 的NaOH溶液.反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图所示.请计算此溶液的溶质质量分数.
的NaOH溶液.反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图所示.请计算此溶液的溶质质量分数.
【答案】24%
【解析】
标签上可以看出该溶液是硫酸镁溶液,向硫酸镁溶液中加入氢氧化钠溶液会发生如下反应:MgSO4+2NaOH=Na2SO4+Mg(OH)2↓。但必须注意的是,参加反应的只是溶液中的溶质,而溶剂水是不参加反应的。我们再来看看关系图,发现:当加入NaOH溶液的质量是40g时,两者恰好完全反应。则参加反应的NaOH的质量是(注意参加两个字)40g×10%,由参加反应的NaOH的质量就可以求出参加反应的硫酸镁的质量(即硫酸镁溶液中溶质的质量)。
解:反应恰好完成时所用NaOH的质量:40g×10%=4g
设25g硫酸镁溶液中溶质的质量为x
MgSO4+2NaOH=Na2SO4+Mg(OH)2↓
120 80
x 4g
![]()
x=6g
硫酸镁溶液中溶质质量分数为:![]() ×100%=24%,
×100%=24%,
答:该硫酸镁溶液中溶质质量分数为24%。

 阅读快车系列答案
阅读快车系列答案【题目】某些铜制品在空气中久置,表面生成绿色的铜锈(又称铜绿)。某化学实验小组设计并进行实验,探究铜锈的组成和铜生锈的条件。
I.探究铜锈的组成
(查阅资料)①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
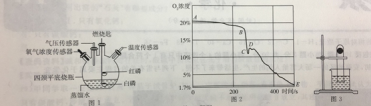
(进行实验)小组同学从铜器上取下适量的干燥铜锈,按图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。
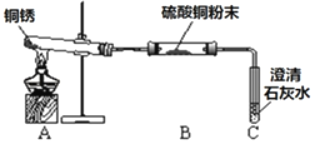
(解释与结论)依据以上现象分析,铜锈中一定含有的元素:Cu和_____。
II.探究铜生锈的条件
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
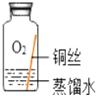
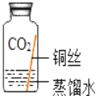
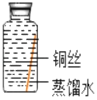
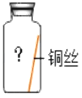
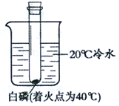
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面 有绿色物质 | 无明显现象 | 无明显现象 |
(解释与结论)
(1)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是_____。
(2)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验②和③,得出的结论是_____。
(4)为验证猜想,实验⑤的集气瓶中的气体是_____。
(5)由上述实验可推知,铜生锈的条件是_____。
(反思与应用)
(6)防止金属锈蚀的方法是_____(写一种)。