��Ŀ����
����Ŀ�����������ڹ����������ճ������еõ��ձ�㷺��Ӧ��
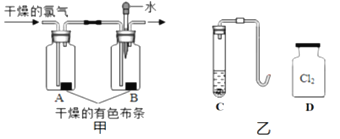
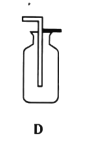
��1������ͼ��ʾʵ��̽���������������ÿ֧�Թ��о�������ȫ��ͬ�Ľྻ��Ƭ����
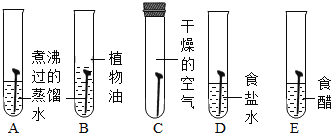
����ͬѧ��Ϊ���Թ�A������������ܹ�˵��������ʴ����������е�������ˮ������ͬ���õĽ������ͬѧ��ͬ�����Ĺ۵㣬��Ϊ����ȫ��۲��Թ�_______��ѡ���Թܱ�ţ�����������������ѧ�Ͻ������������ܵó��������ۡ�B��ֲ���͵�������_______��
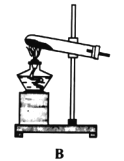
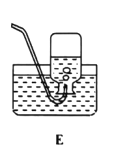
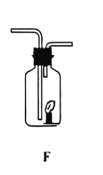
���Թ�D��Eʵ���Ŀ���ǽ�һ��̽������_______�Ļ������Ƿ��������ʴ��
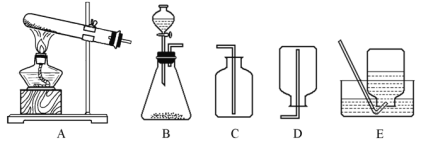
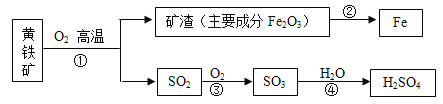
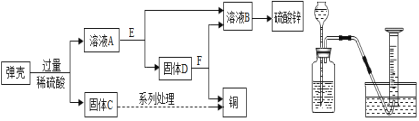
��2����ͭ��ͭп�Ͻ��������ǵ����졣����һ��ʹ�ù��ģ��⼣�߰ߵĵ��ǣ������������ǿ����Ƶ�����п��ͭ������Ҫ������ͼ����ʾ��
���ռ����ϣ������ϵ�����ҪΪCu2��OH��2CO3������ϡ���ᷴӦ�õ�����ͭ��Һ���������������ʲ�����ˮ��Ҳ���μӷ�Ӧ��
�� ��
��д�������ϵ�����ϡ���ᷴӦ�Ļ�ѧ����ʽ_______��
������DΪ_______�����۵ĽǶ�������A��E�ķ�Ӧ��ʵ����_______��
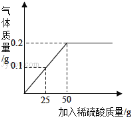
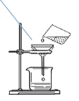
��3��Ϊ�˱Ƚϼס������ֽ����Ļ��ǿ�������ԭ��������С��С������һ��ʵ��װ�ã���ͼ�ң�����ȡ���ֽ�����m�ˣ��ֱ����������ϡ������з�Ӧ������ͬ�����²ⶨ��ͬʱ�����ռ��������������ʵ���¼�����
��Ӧʱ�䣨�룩 | 20 | 40 | 60 | 80 | 100 | 120 | 140 | |
�ռ�������������������� | ���� | 25 | 60 | 95 | 130 | 160 | 170 | 170 |
�ҽ��� | 30 | 75 | 120 | 150 | 150 | 150 | 150 | |
����ʵ������֪��������Խ�ǿ����_______��ʵ���У�����Ҫ�������ֽ�����������ȣ�����Ҫ���Ƶı�����_______��
��Ϊ��ʹ�õ���ʵ������ȷ��С껿�ʼ�ռ������ʱ���Ӧ����_______������ĸ��
A.���ܿ�һ������ð��ʱ B.ð�����������Ҿ���ʱC.������������崿��ʱ
����������ʵ�����ݣ�Ҫ�Ƚϼס������ֽ��������ԭ��������С������֪����������______��
���𰸡�ABC�������� �������������� ����Һ������ Cu2��OH��2CO3+2H2SO4��2CuSO4+3H2O+CO2�� п��ͭ�Ļ���� Zn+Cu2+��Zn2++Cu �ҽ��� ������״̬��ͬ����Ӧ��ʱ����ͬ A ��ͬ�����Ľ������������ᷴӦ��������������Ķ���
��������
��1������ͼ��ʾʵ��̽����������������� ��ͬѧ��Ϊ���Թ�A������������ܹ�˵��������ʴ����������е�������ˮ������ͬ���õĽ������ͬѧ��ͬ�����Ĺ۵㣬��Ϊ����ȫ��۲��Թ�ABC����������������ѧ�Ͻ������������ܵó��������ۣ�����ABC��
B��ֲ���͵������Ǹ���������������̽�����ܷ����⣬�������������������
�� �Թ�D��Eʵ���Ŀ���ǽ�һ��̽����������Һ�����ԵĻ������Ƿ��������ʴ����������Һ�����ԡ�
��2���� Cu2��OH��2CO3��ϡ���ᷴӦ��������ͭ��ˮ�Ͷ�����̼���ʷ�Ӧ�Ļ�ѧ����ʽдΪ��Cu2��OH��2CO3+2H2SO4��2CuSO4+3H2O+CO2����
�� ������ͼ��֪����ҺAΪ����ͭ��ϡ����Ļ��Һ��EΪп��������ͭ��Ӧ��������п��ͭ��Ϊ������ͭ�е�ͭȫ���û������������п�ǹ����ģ����Թ���DΪп��ͭ�Ļ�������п��ͭ�Ļ���
���۵ĽǶ�������A��E�ķ�Ӧ��п������ͭ��Ӧ��������п��ͭ����ʵ��пԭ���û�������ͭ�е�ͭ���ӳ�Ϊͭԭ�ӣ�пԭ��������п���ӣ��ɱ�ʾΪ��Zn+Cu2+��Zn2++Cu������Zn+Cu2+��Zn2++Cu��
��3���� ��ͼ��֪�������ֽ������μӷ�Ӧ��80���ڣ��ҽ������ɵ������������˵���ҽ����Ļ��ǿ�����Խ�����Խ�ǿ�����ҽ����������ҽ�����
ʵ���У�����Ҫ�������ֽ�����������ȣ�����Ҫ���Ƶı����У�������״̬��ͬ����Ӧ��ʱ����ͬ�����������״̬��ͬ����Ӧ��ʱ����ͬ��
��Ϊ��ʹ�õ���ʵ������ȷ����Ӧһ��ʼ��Ҫ����������������������С껿�ʼ�ռ������ʱ���Ӧ���ǣ����ܿ�һ������ð��ʱ������A��
����������ʵ�����ݣ�Ҫ�Ƚϼס������ֽ��������ԭ��������С������֪���������ǣ���ͬ�����Ľ������������ᷴӦ��������������Ķ��٣�������ͬ�����Ľ������������ᷴӦ��������������Ķ��١�