题目内容
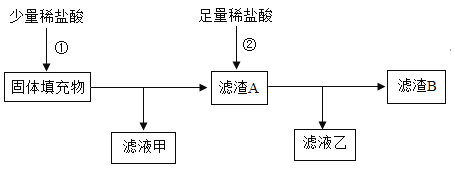
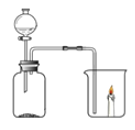
【题目】现有一包黑色粉末,可能含有铁粉、木炭粉、二氧化锰中的一种或几种。请根据以下实验流程图进行推断:
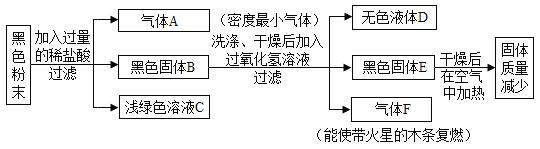
(1)气体A是 _____。
(2)写出生成气体F的化学方程式_____ 。
(3)C溶液是_____ 。
(4)推断这包黑色粉末的成分_____。
【答案】H2 2H2O2![]() 2H2O+O2↑ 氯化亚铁、盐酸 (或FeC12、HCl) 铁粉、木炭粉、二氧化锰的混合物
2H2O+O2↑ 氯化亚铁、盐酸 (或FeC12、HCl) 铁粉、木炭粉、二氧化锰的混合物
【解析】
根据生成的气体A是密度最小的气体,可知A是氢气,由于铁与盐酸可生成氢气和氯化亚铁,所以黑色固体中含有铁,浅绿色的溶液中一定含有氯化亚铁,由黑色固体B能与过氧化氢混合后生成无色的气体F,F能使带火星的木条复燃,则F是氧气;所以该黑色固体中一定含有二氧化锰,含有二氧化锰的黑色固体E在干燥的空气中加热固体质量减少,则说明固体中含有碳,这是因为碳能与空气中的氧气反应生成二氧化碳,从而使固体的质量减小。
(1)由分析可知,A是H2;
(2)气体F(氧气)是双氧水在二氧化锰作催化剂的情况下产生的,其方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)浅绿色的溶液是铁和过量的盐酸反应后生成的氯化亚铁(FeC12)及剩余的盐酸(HCl))溶液;
(4)由以上的分析可知,该黑色粉末中是铁粉、木炭粉、二氧化锰三种物质的混合物。

练习册系列答案
相关题目